微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (9分)实验室用Na2SO4・10H2O配制500ml,0.100mol/L的Na2SO4溶液
(1)所需主要仪器为:药匙、托盘天平、烧杯、胶头滴管、?????????、???????。
(2)本实验须称量硫酸钠晶体(Na2SO4・10H2O)为???????g。
(3)用Na2SO4・10H2O配制标准溶液的正确顺序是???????????????????????????。
A.冷却
B.称量
C.洗涤
D.定容 E.溶解 F.摇匀 G.移液
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不变”)
①没有洗涤烧杯和玻璃棒。????????????。
②定容时俯视容量瓶的刻度线。???????????。
2、实验题 某校化学研究性小组,利用下列提供的实验装置和试剂对某种燃煤所
含元素进行定性和定量检测,试回答:
 ?
?
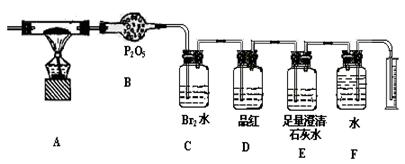
(1)将燃煤充分燃烧,产生气体经化学分析主要含有CO2、H2O、SO2、N2四种气体,则该燃煤一定含有的元素为????????????????.
(2)称取该燃煤样品Wg,通入纯氧使其充分燃烧,检测该燃煤中所含上述元素的质量分数。利用下列装置进行实验:
①指出上述装置中B、C、D、E的作用
B???????????????????????????C????????????????????????
D???????????????????????????E???????????????????????
②为了准确测量F中收集到的气体体积并能根据实验时温度、压强计算其物质的量,正确的实验操作是???????????????????????????????????????????????
3、实验题 (12分)纯净的过氧化钙(CaO2)难溶于水、乙醇,常温下较为稳定。CaO2・8H2O在0℃时稳定,加热至130℃时逐渐变为无水CaO2。在实验室可用钙盐制取CaO2・8H2O,再经脱水制得CaO2。其制备过程如下:
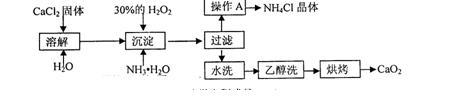
根据以上信息,同答下列问题:
(1)用上述方法制取CaO2・8H2O的化学方程式是???????????;
(2)操作A的步骤为???????????????;
(3)检验“水洗”已经洗净的方法是????????????????????????;
(4)测定产品中CaO2的含量的实验步骤是(己知:I2+2S2O32-=2I-+S4O62-):
第一步:准确称取a g产品于锥形瓶中,加入适量蒸馏水和过量的b g KI品体,再滴入适量2 mol・L-1的H2SO4溶液,充分反应:
第二步:向上述锥形瓶中加入几滴淀粉溶液:
第三步:逐滴加入浓度为c mol・L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。
①第三步反应完全时的现象为???????????;
②产品中CaO2的质量分数为????????????(用字母表示);
③某同学经实验测得产品中CaO2的质量分数偏高,造成偏高的原因是(测定过程中由操作产生的误差忽略不计,用离子方程式表示)??????????????????。
4、选择题 下列制备和收集气体的实验装置合理的是[???? ]
A.用氯化铵和氢氧化钙制取NH3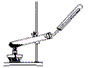
B.用铜片和稀硝酸制取NO 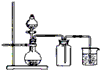
C.用锌粒和稀硫酸制取H2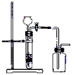
D.用双氧水和二氧化锰制取O2
5、实验题 现某实验需要480 mL 0.2 mol/L的Na2CO3溶液,现用Na2CO3・10H2O晶体配制该溶液。?
(1)① 实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少??????????????????;
② 实验中两次用到玻璃棒,其作用分别是??????????????、??????????????。
(2) 应称取Na2CO3・10H2O晶体的质量为:?????????????。??
(3)根据下列操作对所配溶液的浓度各有什么影响,将其序号填在下面空格:?
①碳酸钠失去了部分结晶水;????②用“左码右物”的称量方法称量晶体;
③碳酸钠晶体不纯,其中混有氯化钠;?④容量瓶中原有少量蒸馏水。?
⑤定容时俯视液面;?⑥摇匀后发现液面低于刻度线再加水。
其中引起所配溶液浓度:a.偏高的有??????????????????????????????;
b.偏低的有??????????????????????????????;
c.无影响的有????????????????????????????。