微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在容积固定的密闭容器中进行的可逆反应2NO2  ?N2O4达到平衡的标志是( )
?N2O4达到平衡的标志是( )
A.反应停止了
B.容器内气体颜色不变
C.容器内气体总质量不变
D.容器内气体密度不变
参考答案:B
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,A不正确。颜色深浅和浓度有关系,所以B正确。根据质量守恒定律可知,气体的质量始终是不变的,C不正确。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,D不正确。答案选B。
本题难度:一般
2、选择题 在一定条件下的密闭容器中,加入2molSO2和1molO2,充分反应后能证明反应:2SO2(g)+O2(g)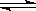 2SO3(g) 是可逆反应的事实是
2SO3(g) 是可逆反应的事实是
A.O2仍为1mol
B.SO2仍为2mol
C.SO2完全转化为 SO3
D.SO2、O2、 SO3同时存在
参考答案:D
本题解析:
试题分析:可逆反应中反应物的转化率不可能是100%的,据此可知,只要容器内SO2、O2、 SO3同时存在,即可证明该反应是可逆反应,答案选D。
点评:该题主要是考查学生对可逆反应特点以及判断依据的了解掌握情况,旨在巩固学生的基础,提高学生分析、归纳、总结问题的能力。有利于培养学生的逻辑思维能力和抽象思维能力。
本题难度:一般
3、填空题 铁及其化合物在生产、生活中应用广泛。
(1)一定条件下,Fe与CO2可发生反应:
2Fe(s)+3CO2(g) Fe2O3(s)+3CO(g)
Fe2O3(s)+3CO(g)
该反应的平衡常数(K ) 随温度(T ) 升高而增大。
①该反应的平衡常数K=______。(填表达式)
②下列措施中,能使平衡时c(CO)/c(CO2) 增大的是????(填标号)。
A.升高温度
B.增大压强
C.充入一定量CO
D.再加一些铁粉
(2)图1装置发生反应的离子方程式为?????????????????????????????????????????。

(3)图2装置中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。

① 电源的M端为?????极,甲烧杯中铁电极的电极反应为????????????????????。
② 乙烧杯中电解反应的化学方程式为?????????????????????????????????????。
③ 停止电解,取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g,甲烧杯中产生的气体标准状况下体积为??????mL 。
参考答案:(1)① 本题解析:
本题解析:
试题分析:(1)①Fe与Fe2O3为固体,不列入平衡常数表达式。
②升高温度,平衡向右移动,c(CO)/c(CO2) 增大,A项正确;,因为反应前后气体系数相等,增大压强、充入一定量CO, c(CO)/c(CO2)不变,故B项、C项不正确;再加铁粉,平衡不移动,D项不正确。
(3)①石墨电极附近变红,H2O电离出的H+放电,使OH?浓度增大,该电极为阴极,所以N极为负极,M极为正极;甲烧杯中铁电极为阳极,Fe失电子:Fe - 2e-=Fe2+。
②电解CuSO4溶液生成Cu、O2、H2SO4,方程式为:2CuSO4+2H2O 2Cu +O2↑ +2H2SO4。
2Cu +O2↑ +2H2SO4。
③Cu电极:Cu2++2e?=Cu,n(e?)=2n(Cu2+)=2×0.64g÷64g/mol=0.02mol,串联电路中通过的电量相等,甲烧杯中石墨电极产生H2:2H++2e?=H2↑V(H2)=1/2n(e?)×22.4L/mol=0.224L=224ml。
本题难度:一般
4、选择题 在10℃时某化学反应速率为0.1mol/(L・min),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6mol/(L・nim),则该反应需在什么温度下进行[???? ]
A.30℃
B.40℃
C.50℃
D.60℃
参考答案:C
本题解析:
本题难度:简单
5、选择题 在密闭容器中发生反应:aX(气)+bY(气) 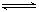 cZ(气)+dW(气),反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中正确的是(???)
cZ(气)+dW(气),反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中正确的是(???)
A.平衡常数K增大
B.a+b<c+d
C.X的转化率下降
D.Z的体积分数增加
参考答案:BC
本题解析:
试题分析:保持温度不变,将容器的容积压缩到原来容积的一半,假定平衡不移动,W浓度变为原来的2倍,达到新平衡时,物质W的浓度是原来的1.8倍,说明平衡向逆反应方向移动,则应由a+b<c+d,据此解答。
A.平衡常数K只与温度有关,即平衡常数K不变,故A错误;
B.平衡向逆反应方向移动,则应由a+b<c+d,故B正确;
C.由上述分析可知,增大压强平衡向逆反应移动,X的转化率下降,故C正确;
D.平衡向逆反应移动,Z的体积分数减小,故D错误;
故选BC。
点评:本题考查化学平衡移动的影响,题目难度不大,本题注意用假定法判断,如果平衡不移动,则达到平衡时W的浓度为原来的2倍,根据实际W的浓度,判断平衡移动。
本题难度:简单