微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 甲、乙、丙三种物质有如下图所示的转化关系。
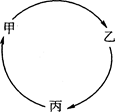
I.若甲、乙、丙依次是氢气、水、硫酸。
(1)写出甲→乙的化学方程式: 。
(2)乙→丙时所需另一种反应物中,一定含有 和氧元素。
Ⅱ.若甲为碳酸钙,丙为氯化钙。
(3)乙可以是 。
Ⅲ.已知难溶性的碱受热会分解生成相应的金属氧化物和水。若甲是铁锈的主要成分,乙的溶液呈黄色。
(4)甲→乙还需要的试剂可以是 。
(5)写出乙→丙的化学方程式: 。
参考答案:(1)2 H2 + O2  本题解析:
本题解析:
试题分析:(1)氢气燃烧生成了水,所以,甲→乙的化学方程式是:2H2+O2 2H2O;
2H2O;
(2)由于水中含有氢、氧元素,并且氢、氧原子的个数比为;2:1,在硫酸中含有氢、硫、氧三种元素,且氢氧原子的个数比是1:2,由质量守恒定律可知,乙→丙时所需另一种反应物中,一定含有硫元素和氧元素;
(3)若甲为碳酸钙,碳酸钙高温受热乙分解生成氧化钙和二氧化碳,氧化钙能与盐酸反应生成氯化钙.所以,乙可能是盐酸;
(4)若甲是铁锈的主要成分,甲在一定条件下转换为乙,乙的溶液呈黄色,则甲为氧化铁,乙为可溶性的铁盐,则甲→乙还需要的试剂可以是盐酸,乙为氯化铁.
(5)由题意可知,甲是氧化铁,可有难溶性的碱丙氢氧化铁受热分解生成,则乙→丙可通过可溶性的铁盐与可溶性的碱反应制取,根据上述反应,氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠.反应的方程式是:FeCl3+3NaOH
本题难度:一般
2、选择题 下列说法中正确的是
A.纯净物一定由分子构成
B.混合物肯定由两种以上元素组成
C.同种分子构成的物质一定是纯净物
D.含有氧元素的化合物都是氧化物
参考答案:C
本题解析:
试题分析:A.纯净物是指只有一种物质,但不一定是由分子构成的,例如金属钠是由原子构成的,故不选A;B.混合物是指含有两种或两种以上的物质,例如氧气和臭氧是两种物质,但只含有一种元素,故不选B;C.同种分子的物质一定是一种物质吗,是纯净物,故选C;D.含有两种元素的化合物中有氧元素的为氧化物,如果含有三种元素的,就不是氧化物,故不选D。
考点:纯净物,混合物,氧化物的判断。
本题难度:一般
3、选择题 下表中物质的分类组合正确的是( )
| A
| B
| C
| D
|
强电解质
| Al2(SO4)3
| BaSO4
| HF
| KClO3
|
弱电解质
| H3PO4
| H2O
| CaCO3
| Al(OH)3
|
非电解质
| CO2
| NH3・H2O
| NH3
| HI
参考答案:A
本题解析:A正确;B错,NH3・H2O属于弱电解质;C错,CaCO3属于强电解质;D错,HI属于强电解质;
本题难度:一般
4、选择题 下列说法正确的是
A.Na2O2、Cl2、SO2依次属于电解质、单质、非电解质
B.标准状况下,1 mol Na2O2和22.4 L SO2反应,转移电子数目为NA
C.等物质的量Cl2和SO2同时通入品红溶液,褪色更快
D.在Na2O2中阴阳离子所含的电子数目相等
参考答案:A
本题解析:
试题分析:A.Na2O2在熔融状态能够导电,是电解质,Cl2中仅含有一种元素,是单质,SO2是化合物,在熔融状态不能导电,在水溶液中本身也不能电离产生自由移动的离子,是非电解质,正确;B.标准状况下,1 mol Na2O2和22.4 L SO2反应,转移电子数目为2NA,错误;C.等物质的量Cl2和SO2同时通入品红溶液,会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,产生的物质没有漂白性,因此失去漂白性,错误;D.在Na2O2中阴离子O22-含有电子数目是18个,阳离子Na+含有10个电子,电子数目不相等,错误。
考点:考查物质的结构、性质、分类及应用的知识。
本题难度:一般
5、选择题 已知下列物质的名称分别是
名称
| 硫代硫酸钠
| 多硫化钙
| 过氧化钡
| 超氧化钾
| 化学式
| Na2S2O3
| CaSx
| BaO2
| KO2
根据上述命名规律回答:K2CS3应命名为
A.三硫代碳酸钾 B.多硫碳酸钾 C.过硫碳酸钾 D.超硫碳酸钾
参考答案:A
本题解析:
试题分析:K2CS3是碳酸钾K2CO3中的三个O原子被S原子代替得到的产物,应该名为三硫代碳酸钾,故选项是 A。
考点:考查物质的命名的知识。
本题难度:一般
|
|