微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质在空气中不能被酒精灯点燃的是( )
A.钠块
B.镁条
C.铝片
D.硫粉
参考答案:A.钠块燃烧生成过氧化钠,不符合题意,故A不选;
B.
本题解析:
本题难度:一般
2、填空题 铝是最常见的金属之一。
(1)浓硝酸、浓硫酸可贮存在铝制容器的原因是???????????????????????????。
(2)纳米铝主要应用于火箭推进剂。工业上利用无水氯化铝与氢化铝锂(LiAlH4)在有机溶剂中反应制得纳米铝,化学方程式如下:3LiAlH4+AlCl3="4Al" + 3LiCl + 6H2↑
该反应的氧化剂为???????????????。
(3)氢化铝钠(NaAlH4)是一种重要的储氢材料,已知:
NaAlH4(s)=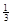 Na3AlH6 (s)+
Na3AlH6 (s)+ 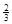 Al (s) + H2(g)????ΔH=+ 37 kJ・molˉ1
Al (s) + H2(g)????ΔH=+ 37 kJ・molˉ1
Na3AlH6(s)="3NaH(s)+" Al (s) + 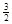 H2(g)??????ΔH=+ 70.5 kJ・molˉ1
H2(g)??????ΔH=+ 70.5 kJ・molˉ1
则NaAlH4(s)=" NaH(s)" + Al (s) +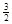 H2(g)??????ΔH=?????????????????。
H2(g)??????ΔH=?????????????????。

(4)已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式 存在。目前研究比较热门的Al-H2O2燃料电池,其原理如右图所示,电池总反应如下:
2Al+3HO2-+3H2O =2[Al(OH) 4]-+OH-
①正极反应式为?????????????????????????。
②与普通锌锰干电池相比,当消耗相同质量的负极活性物质时,Al-H2O2燃料电池的理论放电量约为普通锌锰干电池的______倍。
③Al电极易被NaOH溶液化学腐蚀,这是该电池目前未能推广使用的原因之一。反应的离子方程式为??????????????????????????????。
参考答案:(9分)(1)常温下,铝易被浓硝酸、浓硫酸钝化
(2)
本题解析:
试题分析:(1)常温下,铝易被浓硝酸、浓硫酸钝化,所以浓硝酸、浓硫酸可贮存在铝制容器中。
(2)根据反应的方程式可知,铝元素的化合价从+3价降低到0价,得到电子,发生还原反应,所以氧化剂是LiAlH4、AlCl3 。
(3)根据盖斯定律可知,①+②×1/3,即得到反应式NaAlH4(s)=" NaH(s)" + Al (s) + 本题难度:困难
本题难度:困难
3、填空题 把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀生成,向所得滤液(滤出0.58g沉淀),逐滴加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示[图中的Y表示沉淀质量(g), x表示加入盐酸体积(mL)]
(1) 混合物中NaOH质量是____________g(2`),
MgCl2和AlCl3的物质的量之比是________(2`)
(2) P点所表示的加入盐酸的体积为________ml.(2`)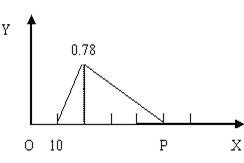
参考答案:(1)2.6g?????? 1:1???? (2)90ml
本题解析:略
本题难度:简单
4、填空题 物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,试回答:
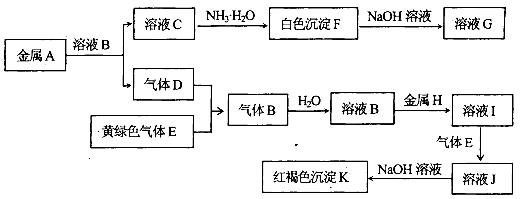
(1)写出下列物质的化学式:气体B是_____________,H是_______________,
(2)写出A与NaOH溶液反应的离子方程式:______________________________________;
(3)写出反应“I→J”的离子方程式:_____________________________________________;
(4)写出反应“F→G”的离子方程式:____________________________________________;
(5)在溶液I中滴入NaOH溶液,可观察到的现象是:_______________________________;
其反应的原理是(化学方程式)_________________________________________________.
(6)检验溶液J中的金属阳离子,用______________________试剂(填化学式),其现象是
_________________________________.
参考答案:
(1)HCl ,? Fe?
(2)2Al+2O
本题解析:
试题分析:K为红褐色沉淀,则应为Fe(OH)3,则溶液J中含有Fe3+,气体E是黄绿色气体判断为Cl2,D应为H2,E应为氧化性气体Cl2,B应为HCl,H为Fe,则I为FeCl2,J为FeCl3,白色沉淀F能溶于过量NaOH溶液,则F为Al(OH)3,G为NaAlO2,A为Al,C为AlCl3,
(1)由以上分析可知B应为HCl? H为Fe?
(2)A与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2 AlO2-+3H2↑
(3)反应“I→J”是FeCl2和Cl2发
本题难度:一般
5、填空题 某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。

请回答下列问题。
(1)?图中涉及分离溶液与沉淀的方法是____________________________。
(2)? B、C、D、E四种物质的化学式为:
B__________、C__________、D__________、E__________。
(3) 写出下列反应的离子方程式:
沉淀F与NaOH溶液反应________________________________。
沉淀E与稀硫酸反应____________________________。
溶液G与过量稀氨水反应________________________________。
参考答案:(1) 过滤??(2) B:? Al2O3?? C:? Fe
本题解析:
试题分析:Al2(SO4)3、Al2O3和Fe2O3中Al2(SO4)3溶于水,Al2O3溶于NaOH,可确定B:? Al2O3?? C:? Fe2O3?? D:? NaAlO2?? E: Al(OH)3。
本题难度:一般