微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铝不易被腐蚀,其主要原因是因为铝?????? (??? )
A.是一种轻金属
B.金属活动性比镁弱
C.具有高熔点
D.易形成致密的氧化物薄膜
参考答案:D
本题解析:考查铝的性质,由于铝是活泼金属,常温下即可被氧气氧化,在其表面形成致密的氧化物薄膜,阻止了它的继续氧化,故选D
本题难度:简单
2、填空题 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题

(1)④、⑤、⑥的原子半径由大到小的顺序是_____________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应
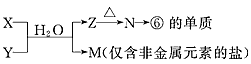
X溶液与Y溶液反应的离子方程式为______________________,N→⑥的单质的化学方程式为_________________________,常温下,为使0.1 mol/L M溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至___________。
参考答案:(1)Na>Al>O
(2)HNO3&g
本题解析:
本题难度:一般
3、选择题 把等质量的金属镁分别放在(1)氧气,(2)空气,(3)二氧化碳气体中完全燃烧,得到的固体质量分别是W1、W2、W3,三者的大小关系是( ? )
A.W1>W2>W3
B.W1=W2=W3
C.W3>W1>W2
D.W3>W2>W1
参考答案:C
本题解析:
本题难度:简单
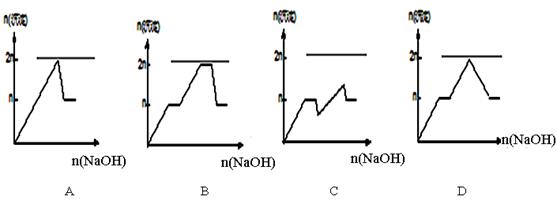
4、选择题 含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是(离子(或物质)沉淀pH见下表)
离子
| Mg2+
| Al 3+
| 物质
| Al(OH)3
|
开始沉淀pH
| 8.93
| 3.56
| 开始溶解pH
| 8.04
|
完全沉淀pH
| 10.92
| 4.89
| 完全溶解pH
| 12.04
参考答案:C
本题解析:
试题分析:根据Mg2+、Al3+开始沉淀时的pH值可知,向MgCl2、AlCl3的混合溶液中滴NaOH溶液首先是氢氧化铝开始沉淀,当氢氧化铝开始溶解时Mg2+还没有开始形成沉淀。当pH=8.93时Mg2+开始形成沉淀,当pH=10.92时Mg2+完全沉淀此时氢氧化铝还没有完全溶解。当pH超过12.04时氢氧化铝完全溶解,因此符合反应过程的图像应该是C,答案选C。
本题难度:一般
5、计算题 两份质量相等且组成完全相同的镁-铝合金,一份投入足量的稀硫酸中,生成氢气的体积是7.84L;另一份投入足量的氢氧化钠溶液,生成氢气的体积是3.36L(以上体积数据均在标准状况下测得)。计算这种镁-铝合金中镁的质量分数。
参考答案:64.0%
本题解析:略
本题难度:简单
|