微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列变化中破坏离子键的是? [???? ]
A、NaOH溶于水 ??????????????????????
B、HCl溶于水 ???
C、SiO2熔化 ??????????????????????????
D、酒精溶于水
参考答案:A
本题解析:
本题难度:简单
2、填空题 已知A、J、D、E、G是元素周期表中1~36号元素,其原子序数依次增大。A与另外四种元素既不在同一周期,也不在同一主族。J和D同主族,E和G同周期;元素G是周期表中的第7列元素,E的最外层电子数与最内层电子数相同,E跟J可形成离子化合物,其晶胞结构(其中J原子在晶胞内部)如图。
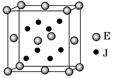
请回答下列问题:
(1)D元素-1价离子的电子排布式为???????????????????????;G元素原子的价电子排布式为???????????????????????????。
(2)元素J与氮元素可以形成化合物NJ3,其中N―J键的化学键类型为???????,根据价层电子对互斥理论可以判断NJ3的空间构型为???????,NJ3分子中N原子的杂化方式为???????杂化。
(3)A、J形成的化合物AJ的相对分子质量比A、D形成的化合物AD的相对分子质量小,但AJ的沸点比AD高,其原因是?????????????????????????。
(4)从晶胞图可以得出:E与J形成的离子化合物的化学式为??????????????。
(5)含有E元素的化合物焰色反应为?????色,焰色反应的原理是??????????。
参考答案:(1)1s22s22p63s23p6(2分) ? 3d54s
本题解析:
试题分析: A与另外四种元素既不在同一周期,也不在同一主族。判断A是H元素;元素G是周期表中的第7列元素,则G是周期表中第四周期第七副族元素Mn元素;E和G同周期,E的最外层电子数与最内层电子数相同,最内层电子数是2,所以E是Ca元素;E跟J可形成离子化合物,通过计算其晶胞结构中E与J的离子个数比是1:2,则J是-1价非金属;J和D同主族,所以J和D应为F、Cl元素。
(1)Cl元素-1价离子的电子排布式为1s22s22p63s23p6,G是25号Mn元素,其价电子排布式为3d54s2
本题难度:一般
3、选择题 某元素的3p能级上有两个未成对电子,因此其( )
A.第三电子层上有4个电子
B.最高正价为+6
C.最高正价为+4
D.是非金属元素
参考答案:元素的3p能级上有两个未成对电子,该元素原子最外层电子排布式
本题解析:
本题难度:一般
4、选择题 某种具有净水作用的无机高分子混凝剂的化学式可以表示为 [Al2(OH)nClm・yH2O]x ,式中的m等于 [???? ]
A、3-n
B、6-n
C、n+6
D、n+3
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列化学用语正确的是 [???? ]
A.聚丙烯的结构简式为: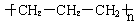
B.丙烷分子的比例模型为: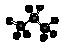
C.四氯化碳分子的电子式为: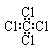
D.CH2=C(CH3)-CH=CH2的名称是:2-甲基-1,3-丁二烯
参考答案:D
本题解析:
本题难度:简单