微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)人类的生活和生产活动,可以说都离不开能源。在 ①石油、②电能、③风能、④煤、⑤天然气、⑥秸杆、⑦水力、⑧水煤气这些能源中,属于“二级能源”的是 ;属于“不可再生能源”的是 。(填序号)
(2)甲、乙两种金属: ①甲单质能与乙盐的溶液反应; ②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙; ③分别与氯气反应生成金属阳离子时,甲失去电子数比乙多;④甲、乙两元素的单质和盐酸组成原电池,乙单质表面生成氢气。其中一定能说明甲的金属性比乙强的有 。(填序号)
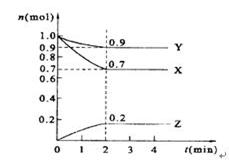
(3)某温度时,在2 L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示。由图中所给数据进行分析,该反应的化学方程式为 ;反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= ;反应达到平衡时,Y的浓度为 。
参考答案:(每空1分,共6分。答不全或有错误选项的不得分,不写单位或单
本题解析:
试题分析:(1)二级能源是指需要依靠其它能源(也就是一级能源)的能量间接制取的能源,电能、水煤气均属于“二级能源”,不可再生能源泛指人类开发利用后,在现阶段不可能再生的能源资源,如石油、煤炭、天然气等,故属于“二级能源”的是②⑧,属于“不可再生能源”的是①④⑤。
(2)④乙单质表面生成氢气,说明乙是正极,即甲的金属性大于乙的金属性。故选④
(3)根据化学计量数之比等于反应的物质的量之比,故方程式为3X+Y 2Z。
2Z。
v(Z)=△c(Z)÷t=△n(Z) ÷V÷t=0.2mol÷2L÷2min=0.05mol/(L・min)。
平衡时,Y的物质的量为0.9mol,体积为2L,浓度为0.9mol/2L=0.455mol/L。
考点:常见能源的种类及其工作原理 金属性强弱比较 化学反应速率和化学平衡
点评:本题考查学生二级能源和不再生能源的概念,可以根据所学知识进行回答,难度不大。
本题难度:一般
2、填空题
|
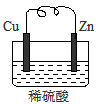
由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀,一段时间后某极产生3.36L(标准状况)的气体。
问:
(1)负极是_________(填“锌”或“铜”),发生_________反应(填“氧化”或“还原”)。
(2)正极的电极反应为______________________
(3)产生这些气体共需转移电子___________mol。
参考答案:(1)锌;氧化
(2)2H++2e-==H2↑
本题解析:
本题难度:一般
3、选择题 下列关于下图所示原电池装置的叙述中,正确的是

A.铜片是负极
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.氢离子在铜片表面被还原
参考答案:D
本题解析:
试题分析:A、该原电池中Zn作负极,Cu作正极,错误;B、正极发生还原反应,所以Cu极有氢气放出,铜片质量不变,错误;C、外电路电流从正极流向负极,所以电流从锌片流向铜片,错误;D、氢离子在正极被还原,正确,答案选D。
本题难度:一般
4、填空题 (12分)(1)物质的量浓度相同的三种盐NX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是 。
(2)比较下列溶液的pH(填“>”“<”或“=”):
①0.1 mol・L-1Na2CO3溶液 0.1 mol・L-1NaHCO3溶液
②0.1 mol・L-1NH4Cl溶液 0.01 mol・L-1NH4C1溶液
(3)把a、b、c、d四块金属片浸泡在稀H2SO4中,用导线两两相连,可以组成各种原电池。若a、b相连,a为负极;c、d相连,c极发生氧化反应;a、c相连,c为正极;b、c相连,电流由c极流向b极,则这四种金属的活动性由强到弱的顺序为 。
(4)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成份是 。
(5)氯化铁溶液呈 性(填“酸”、“碱”或“中”),原因是(用离子方程式表示):
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,溶液的pH 7(填“>”“<”或“=”),离子反应总方程式为: 。
参考答案:(1)HX>HY>ZH;(2)① &
本题解析:
试题分析:(1)物质的量浓度相同的三种盐,pH越大,说明酸根离子水解越是强烈,对应的酸越弱,所以HX、HY、HZ的酸性由强到弱的顺序为HX>HY>HZ;(2)①同浓度的Na2CO3和NaHCO3溶液,CO32-水解程度大于 HCO3-所以0.1 mol・L-1Na2CO3溶液的pH>0.1 mol・L-1NaHCO3溶液的pH,②不同浓度的NH4Cl溶液,浓度越小,NH4+水解程度越大,但是水解后溶液的酸性越弱。所以②0.1 mol・L-1NH4Cl溶液的pH<0.01 mol・L-1NH4C1溶液的pH;(3)组成各种原电池。若a、b相连,a为负极;活动性a>b,c、d相连,c极发生氧化反应为负极,活动性c>d;a、c相连,c为正极, a>c,b、c相连,电流由c极流向b极,活动性b>c,综上:a >b>c>d;(4) AlCl3溶液蒸干得到氢氧化铝,灼烧得到氧化铝。(5) 氯化铁溶液呈酸性,因为Fe3+水解,Fe3++3H2O Fe(OH)3+3H+;(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,发生的反应如下Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O.得到的是NaAlO2溶液,溶液的pH<7。
Fe(OH)3+3H+;(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,发生的反应如下Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O.得到的是NaAlO2溶液,溶液的pH<7。
考点:考查盐类的水解的应用和金属活动性比较。
本题难度:困难
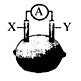
5、选择题 下图所示的柠檬水果电池中,外电路上的电子从电极Y流向电极X。若X为铅电极,则Y可能是
A.锌
B.银
C.石墨
D.铜
参考答案:A
本题解析:
原电池的两极的活性必须不同.外电路上的电子从电极Y流向电极X,则电极X的活性要大于电极Y的活性. 因X为铅电极,则Y电极的活性要强于铅,银、石墨、铜的活性与铅相近,锌比较适合。
故正确答案为A
本题难度:一般