微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 为了避免青铜器生成铜绿,以下方法正确的是[???? ]
A.将青铜器放在银质托盘上
B.将青铜器与直流电源的正极相连
C.将青铜器保存在潮湿的空气中
D.在青铜器的表面覆盖一层防渗的高分子膜
参考答案:D
本题解析:
本题难度:简单
2、选择题 海水中溶解和悬浮着大量的无机物与有机物,具有巨大的开发潜力,人类除了从海水中获得食盐和水外,还获得大量的钾、镁、溴、碘等,以下说法不正确的是?????????????(???)
A.钾与溴两种元素位于周期表中同一周期,二者形成的化合物中只有离子键
B.轮船在海水中与在江河中航行相比,在海水中更易被腐蚀
C.若氯有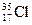 、
、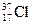 两种核素,则
两种核素,则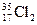 、
、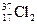 化学性质几乎相同
化学性质几乎相同
D.海水中的上述元素变成单质状态过程中,均发生了氧化反应
参考答案:D
本题解析:钾是活泼金属,溴是活泼非金属,二者能形成离子键,A对;轮船在海水中易形成原电池,加速了轮船的腐蚀速率,B对;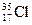 、
、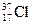 的电
的电
本题难度:简单
3、选择题
A.4Fe(OH)2+2H2O+O2===4Fe(OH)3↓
B.2Fe+2H2O+O2===2Fe(OH)2↓
C.2H2O+O2+4e-===4OH-
D.Fe-3e-===Fe3+
参考答案:D
本题解析:洗过的铁锅在空气中放置,可发生吸氧腐蚀。负极发生的反应为2Fe-4e-==2Fe2+,正极发生的反应为2H2O+O2+4e-===4OH-,总反应式为2Fe+2H2O+O2===2Fe(OH)2,而Fe(OH)2又被O2氧化为红褐色的Fe(OH)3。
本题难度:简单
4、填空题 (8分)钢铁的生产与使用是人类文明和生活进步的一个重要标志。
(1)工业铝热法炼铁的主要化学反应方程式????????????????????????。
(2)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。试回答:①铁锅的腐蚀主要是由??????????腐蚀造成的。
②铁锅锈蚀的负极反应式为?????????????????????????????。
(3)通常使用钢铁是铁和__________的合金;当马口铁(表层镀锡)镀层被损坏后,这时被腐蚀速度比普通铁_______(填“快”或“慢”)。为防止轮船的船体在海水中腐蚀,一般在船身连接???????????(填“锌块”或“铜块”)
参考答案:(1)2Al+Fe2O3=Al2O3+2Fe
(2)
本题解析:
试题分析:(1)铝热法炼铁的化学反应方程式:2Al+Fe2O3=Al2O3+2Fe
(2)炒过菜的铁锅未及时洗净(残液中含NaCl),因此属于吸氧腐蚀。负极反应为:Fe - 2e =Fe2+。
(3)钢铁是铁和碳的合金,马口铁破损后由于锡的活泼性比铁差,因此铁的腐蚀速度比普通铁快,要防止轮船的船体腐蚀,应用锌块来保护铁。
点评:本题比较综合,但是比较基础,难度适中。
本题难度:一般
5、选择题 我们在学习和生活过程中所观察的以下现象与电化腐蚀有关的是
A.光亮的自行车钢圈不易生锈
B.炒过菜的铁锅未及时洗净出现红褐色锈斑
C.光亮的铜丝在火焰上灼烧后变黑
D.实验室镁带拆封放置一段时间后表面变灰暗
参考答案:B
本题解析:自行车钢圈属于合金,不易生锈;铜加热时被氧化生成黑色氧化铜;镁是活泼的金属,极易被氧化,这些都是与电化学腐蚀无关系的。选项B中是钢铁的电化学腐蚀,所以答案选B。
本题难度:简单