��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���е���ʽ�У���д��ȷ����
�ο��𰸣�B
���������������ԭ�ӻ���û�в���ɼ��ĵ��ӣ�����ʽΪ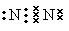 ���Ȼ��ƺ��������ƾ������ӻ��������ʽ�ֱ�Ϊ
���Ȼ��ƺ��������ƾ������ӻ��������ʽ�ֱ�Ϊ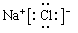 ��
�� �����Ѷȣ�һ��
�����Ѷȣ�һ��
2��ѡ���� �����¶��ܼӿ컯ѧ��Ӧ���ʵ���Ҫԭ����
A.���ӷ�����ײ����
B.���ӷ��ӵ�����
C.�����˷�Ӧ���������
D.���ӷ�Ӧ���л���ӵİٷ���
�ο��𰸣�D
�����������������������¶ȣ��������ṩ�������������˻���ӵ���Ŀ����Ч��ײ�Ļ���ͻ����ӣ����Է�����ײ����Ҳ���ӣ���������Ҫԭ��ѡD��
���㣺�����
��������Ӧ֮�����ܹ���������Ϊ�л���ӵ���Ч��ײ�������¶������ӵĻ���ӵİٷ�����
�����Ѷȣ�����
3��ѡ���� �����������ɷ������·�Ӧ��P4 +5O2=P4O10����֪�������л�ѧ����Ҫ���յ������ֱ�Ϊ��P-P
akJ��mol-1��P-O b kJ��mol-1��P=O c kJ��mol-1�� O=O d kJ��mol-1�� ������ͼ��ʾ�ķ��ӽṹ���й����ݹ���÷�Ӧ�ġ�H��������ȷ����?
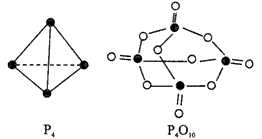
[???? ]
A. (6a+5d -4c -12b)kJ��mol-1
B. (4c+12b -6a -5d)kJ��mol-1
C. (4c+12b -4a-5d)kJ��mol-1
D. (4a +5d -4c - 12b)kJ��mol-1
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� ��14�֣���20g Ba(OH)2��8H2O������10 g NH4Cl����һ�����С�ձ��У����ձ����ڵ���3��4��ˮ�IJ���Ƭ�ϣ��ò�����Ѹ�ٽ��衣
��1��ʵ���в������������� ��
��2��д���йط�Ӧ�Ļ�ѧ����ʽ ��
��3��ʵ���й۲쵽�������� �� �ͷ�Ӧ�����ɺ�״��
��4��ͨ�� ����˵���÷�ӦΪ ������ȡ����ȡ�����Ӧ���������ڷ�Ӧ��������� ���С�ڡ����ڡ������������������
�ο��𰸣���ÿ��2�֣���14�֣�
��1������ʹ������ֽӴ�����
���������
��1������ʹ������ֽӴ�����Ӧ
��2��Ba(OH)2��8H2O��2NH4Cl��BaCl2��2NH3 ����10H2O
��3������Ƭ�Ͻ������С�ձ�ճ��һ���������̼�����ζ
��4����������ȣ�С��
����Ե��͵����ȷ�Ӧ�����˿��飬ѧϰʱע��Ӣ�ʵ��Ŀ�Ģ�ԭ����ԭ�Ϣ�װ�â�ʵ�������ʵ�������ʵ����ۢ�ؼ��������۵ȼ�������������������ڼ�������������
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ������������ԭ��Ӧ����
A.Cu+4?HNO3��Ũ��Cu��NO3��2+2?NO2��+2?H2O
B.Cu+2FeCl3�TCuCl2+2FeCl2
C.��NH4��2SO4+2NaOHNa2SO4+2NH3��+2H2O
D.2FeCl3+SO2+2H2O�TH2SO4+2HCl+2FeCl2
�ο��𰸣�C
����������������е���ת�ƵĻ�ѧ��Ӧ��������ԭ��Ӧ������������Ԫ�ػ��ϼ۵��������ݴ˷������
���A���÷�Ӧ�У�ͭʧ���ӣ�����õ��ӣ������е���ת�ƣ���������ԭ��Ӧ����A��ѡ��
B���÷�Ӧ�У�ͭʧ���ӣ��Ȼ����õ��ӣ������е���ת�ƣ���������ԭ��Ӧ����B��ѡ��
C���÷�Ӧ�У���Ԫ�صĻ��ϼ۶����仯�����Բ���������ԭ��Ӧ����Cѡ��
D���÷�Ӧ�У��Ȼ����õ��ӣ���������ʧ���ӣ������е���ת�ƣ���������ԭ��Ӧ����D��ѡ��
��ѡC��
���������⿼����������ԭ��Ӧ���жϣ���ȷԪ�صĻ��ϼ��ǽⱾ��Ĺؼ����ѶȲ���
�����Ѷȣ�����