微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是
A.1molO2的质量为32g?mol-1
B.1mol物质的质量等于该物质的相对分子质量或相对原子质量
C.SO42-的摩尔质量为96?g?mol-1
D.CO2的摩尔质量为44g
参考答案:C
本题解析:分析:A、质量的单位为g;
B、根据1mol物质的质量在以克为单位时等于该物质的相对分子质量或相对原子质量;
C、摩尔质量以g?mol-1为单位时,其数值等于相对分子质量;
D、摩尔质量的单位为g?mol-1.
解答:A、1molO2的质量为32g,故A错误;
B、1mol物质的质量在以克为单位时等于该物质的相对分子质量或相对原子质量,故B错误;
C、SO42-的相对分子质量为96,所以SO42-的摩尔质量为96?g?mol-1,故C正确;
D、CO2的摩尔质量为44g?mol-1,故D错误;
故选C.
点评:本题主要考查了摩尔质量,需要注意的是1mol物质的质量在以克为单位时等于该物质的相对分子质量或相对原子质量.
本题难度:简单
2、选择题 阿佛加德罗常数用NA表示,下列叙述正确的是
A.室温时,0.1L?1mol?L-1的盐酸,溶液中水电离出的H+数为10-13NA
B.1L?0.2mol?L-1MgSO4溶液中的阳离子数小于0.2NA
C.2.88g?ND2中含有的电子数是0.18NA
D.常温常压下,3g?HCHO和CH3COOH混合物中含有0.4NA个原子
参考答案:D
本题解析:分析:A、依据稀酸溶液中离子积常数计算得到;
B、溶液中阳离子为镁离子和氢离子,镁离子水解生成的氢离子,阳离子增多;
C、n= 计算物质的量结合取代基计算电子数;
计算物质的量结合取代基计算电子数;
D、HCHO和CH3COOH最简式相同为CH2O,只需计算3gCH2O中含原子数;
解答:A、室温时,0.1L 1mol?L-1的盐酸,c(H+)=1mol/L;溶液中c(H+)c(OH-)=10-14溶液中水电离出的H+数为10-14NA,故A错误;
B、1L 0.2mol?L-1MgSO4溶液中,Mg2++2H2O?Mg(0H)2↓+2H+;1L 0.2mol?L-1MgSO4溶液中的阳离子数大于0.2NA,故B错误;
C、2.88g ND2中物质的量=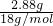 =0.16mol;含有的电子数是0.16mol×9×NA=1.44NA,故C错误;
=0.16mol;含有的电子数是0.16mol×9×NA=1.44NA,故C错误;
D、HCHO和CH3COOH最简式相同为CH2O,只需计算3gCH2O中含原子数=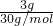 ×4×NA=0.4NA个,故D正确;
×4×NA=0.4NA个,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要是溶液中离子积的计算应用,盐类水解的分析判断,质量换算物质的量计算微粒数,题目难度中等.
本题难度:困难
3、选择题 下列物质中,前者属于氧化物、后者属于电解质的是
A.Al2O3、CaCO3
B.HClO、Cu
C.C2H6O、CH4
D.NO2、NH3
参考答案:A
本题解析:分析:氧化物由负价氧和另外一种元素组成的二元化合物,属于纯净物;水溶液中或熔融状态下能够导电的化合物称为电解质;在上述两种情况下都不能导电的化合物称为非电解质.注意电解质与非电解质都属于化合物,电解质自身可以离解成自由移动的离子,酸、碱、盐都是电解质;非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子.
解答:A.Al2O3由Al、O两种元素组成,且氧元素为负价,属于氧化物;碳酸钙属于盐,属于电解质,故A正确;
B.HClO由三种元素组成,不属于氧化物;Cu属于单质,即不是电解质,也不是非电解质,故B错误;
C.C2H6O由三种元素组成,不属于氧化物;CH4属于共价化合物,不溶于水,液态不导电,属于非电解质,故C错误;
D.NO2由N、O两种元素组成,且氧元素为负价,属于氧化物;NH3属于共价化合物,液态不导电,溶于水导电,是由于与水反应生成一水合氨,一水合氨电离出铵根离子与氢氧根离子,NH3属于非电解质,故D错误;
故选A.
点评:本题考查氧化物、电解质的基本概念,比较基础,注意抓住概念中的关键词理解概念.
本题难度:困难
4、选择题 下列各物质中所含氢原子个数与3.2gO2分子数相同的物质是
A.0.2gNH3
B.6.02×1023个H2SO4分子
C.0.1molHCl分子
D.标准状况下1.12LCH4
参考答案:C
本题解析:分析:利用n= 来计算氧气的物质的量,再利用n=
来计算氧气的物质的量,再利用n= 、n=
、n= 、n=
、n= 及物质的构成来计算氢原子的物质的量,若氢原子的物质的量与氧气的物质的量相等,则个数相同.
及物质的构成来计算氢原子的物质的量,若氢原子的物质的量与氧气的物质的量相等,则个数相同.
解答:3.2gO2的物质的量为 =0.1mol,
=0.1mol,
A、氨气的物质的量为 =0.012mol,氢原子的物质的量为0.012mol×3=0.036mol,故A错误;
=0.012mol,氢原子的物质的量为0.012mol×3=0.036mol,故A错误;
B、H2SO4分子的物质的量为 =1mol,氢原子的物质的量为1mol×2=2mol,故B错误;
=1mol,氢原子的物质的量为1mol×2=2mol,故B错误;
C、0.1molHCl分子中氢原子的物质的量为0.1mol×1=0.1mol,故C正确;
D、标准状况下甲烷的物质的量为 =0.5mol,氢原子的物质的量为0.5mol×4=2mol,故D错误;
=0.5mol,氢原子的物质的量为0.5mol×4=2mol,故D错误;
故选C.
点评:本题考查学生利用n= 、n=
、n= 、n=
、n= 及物质的构成进行的简单计算,明确氢原子的个数与氧分子数相同,即选项中氢原子的物质的量与氧气的物质的量相等是解答本题的关键.
及物质的构成进行的简单计算,明确氢原子的个数与氧分子数相同,即选项中氢原子的物质的量与氧气的物质的量相等是解答本题的关键.
本题难度:困难
5、选择题 下列叙述正确的是
A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.将固体加入容量瓶中溶解并稀释至刻度,配置成一定物质的量浓度的溶液
C.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
D.从碘水中提取单质碘时,不能用无水乙醇代替CCl4
参考答案:D
本题解析:分析:A.稀释浓硫酸时,应将浓硫酸沿烧杯壁缓慢注入水中,并用玻璃棒不断搅拌;
B.不能在容量瓶内溶解或稀释;
C.配制溶液时,若加水超过容量瓶刻度,应倒掉溶液,洗涤容量瓶,重新配制;
D.乙醇与水互溶,不能萃取碘水中的碘.
解答:A.稀释浓硫酸时,应将浓硫酸沿烧杯壁缓慢注入水中,并用玻璃棒不断搅拌,防止液体溅出伤人,故A错误;
B.不能在容量瓶内溶解或稀释,防止放出大量的热,影响溶液的体积,甚至导致容量瓶破裂的危险,故B错误;
C.配制溶液时,若加水超过容量瓶刻度,溶液是均匀,金属用胶头滴管将多余溶液吸出,溶液的浓度偏低,应倒掉溶液,洗涤容量瓶,重新配制,故C错误;
D.乙醇与水互溶,不能萃取碘水中的碘,从碘水中提取单质碘时,不能用无水乙醇代替CCl4,故D正确;
故选D.
点评:本题考查一定物质的量浓度溶液配制、实验基本操作、萃取等,难度不大,注意基础知识的理解掌握.
本题难度:简单