微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 由镁、铝、铁三种金属单质中的两种组成的混合物共6g,与足量的稀盐酸反应,产生标准状况下的氢气2.8L,由此得出的结论中正确的是
A.混合物中一定含有铝
B.混合物中一定含有铁
C.该混合物一定是由铁和镁组成的
D.混合物中一定不含有铁
参考答案:B
本题解析:分析:根据n= 计算氢气的体积,根据电子转移守恒计算提供1mol电子需要金属的平均质量,计算提供1mol电子需要各金属的质量,根据平均值判断.
计算氢气的体积,根据电子转移守恒计算提供1mol电子需要金属的平均质量,计算提供1mol电子需要各金属的质量,根据平均值判断.
解答:标准状况下,2.8L氢气的物质的量= =0.125mol,
=0.125mol,
根据电子转移守恒可知,6g混合金属提供电子的物质的量为0.125mol×2=0.25mol,
故提供1mol电子需要混合金属的平均质量为6g× =24g,
=24g,
镁与盐酸反应表现+2价,提供1mol电子需要Mg的质量为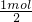 ×24g/mol=12g,
×24g/mol=12g,
铝与盐酸反应表现+3价,提供1mol电子需要Al的质量为 ×27g/mol=9g,
×27g/mol=9g,
铁与盐酸反应表现+2价,提供1mol电子需要Fe的质量为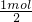 ×56g/mol=28g,
×56g/mol=28g,
Fe提供1mol电子的质量大于24g,Mg、Al提供1mol电子的质量小于24g,故一定含有Fe,Mg、Al至少含有一种,
故选B.
点评:本题考查混合物的有关计算,难度不大,注意利用平均值法与极限法的利用.
本题难度:困难
2、选择题 下列反应中,不属于加成反应的是
A.乙烯与氢气反应制取乙烷
B.甲烷与氯气反应制取一氯甲烷
C.乙烯与氯化氢反应制取氯乙烷
D.乙烯使溴的四氯化碳溶液褪色
参考答案:B
本题解析:
试题分析:根据反应的特点A、C、D属于加成反应,B属于取代反应,所以选B。
考点:有机化学反应类型
点评:取代反应:有机物分子里的某些原子或原子团被其他的原子或原子团所替代的反应。加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。消去反应:有机化合物在一定条件下,从一个小分子中脱去一个或几个小分子,而生成含不饱和键化合物的反应。
本题难度:困难
3、选择题 下列离子方程式与所述事实相符且正确的是
A.H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑
B.用双氧水和稀硫酸处理铜板:Cu+H2O2+2H+=Cu2++2H2O
C.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
D.铵明矾[AlNH4(SO4)2?12H2O]溶液中加入过量氢氧化钡溶液:Al3++NH4++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O
参考答案:BD
本题解析:分析:A.发生氧化还原反应生成NaOH和氧气,水既不是氧化剂也不是还原剂;
B.发生氧化还原反应生成硫酸铜和水;
C.反应生成碳酸钙和HClO;
D.[AlNH4(SO4)2?12H2O]完全反应.
解答:A.H218O中投入Na2O2固体的离子反应为2H218O+2Na2O2=418OH-+O2↑4Na+,故A错误;
B.用双氧水和稀硫酸处理铜板的离子反应为Cu+H2O2+2H+=Cu2++2H2O,故B正确;
C.漂白粉溶液在空气中失效的离子反应为Ca2++2ClO-+CO2+H2O=2HClO+CaCO3↓,故C错误;
D.铵明矾[AlNH4(SO4)2?12H2O]溶液中加入过量氢氧化钡溶液的离子反应为Al3++NH4++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O,故D正确;
故选BD.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意反应的实质,选项A中的氧化还原及D中与量有关的离子反应为解答的难点,题目难度中等.
本题难度:一般
4、选择题 某饱和一元醇8.8g和足量的金属Na反应,生成标准状况下氢气为1.12??L,该醇可氧化成醛,则其结构可能有几种
A.3种
B.4种
C.5种
D.6种
参考答案:B
本题解析:标准状况下氢气为1.12 L,则物质的量是0.05mol,所以一元醇的物质的量是0.1mol,因此一元醇的相对分子质量是88,即为分子式为C5H12O。又因为醇可氧化成醛,说明和羟基相连的碳原子是含有2个氢原子,因此符合条件的醇有4种,分别是1-戊醇,2-甲基丁醇,3-甲基丁醇,2,2-二甲基丙醇。答案选B。
本题难度:困难
5、选择题 在SiO2+3C SiC+2CO↑反应中,氧化剂和还原剂的质量比为
SiC+2CO↑反应中,氧化剂和还原剂的质量比为
A.36:30
B.60:36
C.2:1
D.1:2
参考答案:D
本题解析:分析:SiO2+3C SiC+2CO↑反应中,根据化合价可知,C既是氧化剂又是还原剂,质量之比等于物质的量之比,可有方程式判断氧化剂和还原剂之间的物质的量关系.
SiC+2CO↑反应中,根据化合价可知,C既是氧化剂又是还原剂,质量之比等于物质的量之比,可有方程式判断氧化剂和还原剂之间的物质的量关系.
解答:SiO2+3C SiC+2CO↑反应中,Si元素的化合价反应前后没有变化,当3molC参加反应时,有1molSiC生成,说明1molC起到氧化剂的作用,有2molCO生成,说明有2molC起到还原剂的作用,则氧化剂与还原剂的物质的量之比为1:2,则质量之比为1:2,
SiC+2CO↑反应中,Si元素的化合价反应前后没有变化,当3molC参加反应时,有1molSiC生成,说明1molC起到氧化剂的作用,有2molCO生成,说明有2molC起到还原剂的作用,则氧化剂与还原剂的物质的量之比为1:2,则质量之比为1:2,
故选D.
点评:本题考查氧化还原反应,题目难度不大,注意化合价的变化是解答该题的关键.
本题难度:简单