微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是
A.CaO + H2O = Ca(OH)2
B.3NO2 + 2H2O = 2HNO3+NO
C.2H2O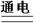 2H2↑+O2↑
2H2↑+O2↑
D.2Na +2H2O =2NaOH+H2↑
参考答案:B
本题解析:略
本题难度:简单
2、选择题 下列各项中表达正确的是
A.H2O2的电子式:
B.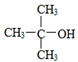 的命名:2,2―二甲基―2―乙醇
的命名:2,2―二甲基―2―乙醇
C.常温下,浓度都为0.1mol・Lˉ1的Na2CO3、NaHCO3溶液的pH,前者小于后者
D. 为二氯化二硫(S2Cl2)的结构,分子中有极性键、非极性键,是极性分子
为二氯化二硫(S2Cl2)的结构,分子中有极性键、非极性键,是极性分子
参考答案:D
本题解析:A 错误,H2O2是共价化合物,电子式中没有中括号
B 错误命名:2-甲基-2-丙醇
C 错误,浓度相同时,碳酸钠的碱性强于碳酸氢钠的碱性,即前者的PH大于后者。
D 正确。
本题难度:一般
3、简答题 把19.2g的Cu放入500mL2mol?L-1稀硝酸中,充分反应,Cu完全溶解.求:
(1)写出Cu与稀硝酸反应的离子方程式:______;
(2)转移电子数目为______(用含NA的式子表示);
(3)氧化剂与还原剂的物质的量比为______.
(4)反应后溶液中C(H+)为______(体积变化忽略不计)
参考答案:(1)Cu与稀硝酸反应生成硝酸铜、NO与水,反应离子方程式为
本题解析:
本题难度:一般
4、选择题 化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是:(???? )?
A.CO2的电子式:
B.质量数为37的氯原子:1737Cl

C.NH4Cl的电子式:
D.原子核内有10个中子的氧原子: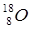
参考答案:D
本题解析:A不正确,CO2分子中含有碳氧双键,电子式为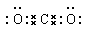 。B不正确,应该是
。B不正确,应该是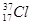 ,C不正确,应该是
,C不正确,应该是 本题难度:简单
本题难度:简单
5、选择题 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知: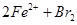 ==2Fe3++2Br-、2Fe3++2I-==2Fe2++I2,下列说法中错误的是
==2Fe3++2Br-、2Fe3++2I-==2Fe2++I2,下列说法中错误的是
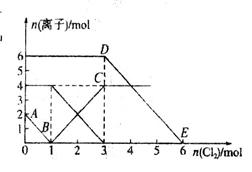
A.还原性:I->Fe2+>Br-
B.线段AB表示Fe2+被氯气氧化
C.线段BC表示生成4 mol Fe3+
D.原溶液中n (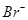 )="6" mol
)="6" mol
参考答案:B
本题解析:
试题分析:A、反应2Fe2++Br2=2Fe3++2Br-中,还原剂Fe2+的还原性强于还原产物Br-,所以还原性:Fe2+>Br-,反应2Fe3++2I-=2Fe2++I2中,还原剂I-的还原性强于还原产物Fe2+,所以还原性:I->Fe2+,所以还原性I->Fe2+>Br-,故A正确;B、通入氯气后,碘离子先被氧化,其次是亚铁离子,最后是溴离子,在通入氯气的量为0~1mol的过程中,碘离子从最大量降到0,即得到碘离子的物质的量为2mol,通入氯气的量为1~3mol的过程中,亚铁离子从4mol降到0,三价铁的量逐渐增大,所以含有亚铁离子共4mol,在通入氯气的量为3~6mol的过程中溴离子从6ml降到0,所以溴离子的物质的量是6mol,即FeBr2的物质的量为3mol,故B错误;根据以上分析可知CD正确,答案选B。
考点:考查氧化还原反应的有关判断与计算
本题难度:一般