微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA代表阿伏加德罗常数的数值,下列说法中正确的是(???)
A.标准状况时,22.4L四氯化碳所含有的分子数为NA
B.34g H2O2中含有的非极性共价键数为 NA
C.碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA
D.将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数为NA
参考答案:B
本题解析:
试题分析:标准状况下,四氯化碳不是气态,不能适用于气体摩尔体积,A不正确;1分子双氧水中含有1个非极性键。34g双氧水的物质的量是1mol,含有的非极性共价键数为 NA,B正确;锌在反应中失去2个电子,1.3g锌的物质的量是0.02mol,转移0.04mol电子,C不正确;选项D中的反应是可逆反应,反应物的转化率不可能是100%的,因此将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数小于NA,D不正确,答案选B。
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考
本题难度:一般
2、实验题 实验室要用98%(密度为1.84g.cm-3)的硫酸配制3.68mol/L的硫酸溶液480mL。
(1)需准确量取98%的硫酸 mL。
(2)要配制3.68mol/L的硫酸溶液480mL,必须用到的仪器是烧杯、玻璃棒、量筒
(3)若配制3.68mol/L的硫酸溶液的其它操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是 。
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的稀硫酸向容量瓶内转移时,因操作不当使部分稀硫酸溅出瓶外
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切
D.用胶头滴管向容量瓶中加水时,仰视观察溶液凹液面与容量瓶刻度相切
(4)若配制时,因加水不慎超过了容量瓶刻度线,此时实验应如何继续进行?
参考答案:(1)100 (2)500mL容量瓶&
本题解析:
试题分析:(1)设需要98%H2SO4的体积为VmL,根据溶液稀释前后溶质质量不变则,VmL×1.84g・cm-3×98%=0.5L×3.68mol・L-1×98g・mol-1,得V=100ml,所以溶液的体积为100ml,答案为:100;(2)配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以仪器有烧杯、玻璃棒、100mL量筒、500mL容量瓶、胶头滴管,答案为:500mL容量瓶、胶头滴管;(3)A.因烧杯内壁沾有溶质,将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质的质量减小,浓度减少,A正确;B.将烧杯内的稀硫酸向容量瓶内转移时,因操作不当使部分稀硫酸溅出瓶外,因溅出稀硫酸中含有溶质,溶质的质量减少,浓度减少,B正确;C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切,因吸出的液体中含有溶质,溶质的质量减少,浓度减少,C正确;D.用胶头滴管向容量瓶中加水时,仰视观察溶液凹液面与容量瓶刻度相切,溶液的液面高于刻度线,溶液的体积偏大,浓度偏小,D正确;(4)因配制时,一旦出现的错误操作,必须重新配制,答案为:重新配制.
考点:配制一定物质的量浓度的溶液
本题难度:一般
3、选择题
A.29∶8∶13
B.22∶1∶14
C.13∶8∶29
D.26∶16∶57
参考答案:CD
本题解析:由于CO与N2具有相同的相对分子质量,所以CO2、H2、CO混合气体的平均相对分子质量仅由CO2和H2来决定,CO的量可以任意。由交叉法:
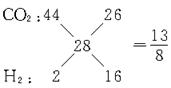
本题难度:简单
4、选择题 NA代表阿伏加德罗常数的值,下列说法正确的是
A.5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA个
B.标准状况下,2.24 L水中含有0.1 NA个水分子
C.1.12 L氯气中含有0.1 NA个氯原子
D.0.1molNa2O2与足量的CO2反应转移的电子数为0.1NA
参考答案:D
本题解析:A错误,5.6 g 铁在足量氯气中燃烧,电子转移0.3NA个,因为生成是+3价铁。
B错误,标准状况下,水是液体。
C错误,没指明气体状态。
D正确,过氧化钠发生自身氧化还原反应,转移电子数为0.1NA。
本题难度:简单
5、选择题 Na2SO4・10H2O的摩尔质量是 ,483g Na2SO4・10H2O中所含Na2SO4・10H2O的物质的量是 ,所含Na+的物质的量是 ,所含H2O分子的数目是 个。
参考答案:(8分,每空2分)
322g/mol,1
本题解析:
试题分析:Na2SO4・10H2O的摩尔质量为:(23×2+32+16×4+10×18)g/mol=322g/mol;483g Na2SO4・10H2O中所含Na2SO4・10H2O的物质的量为:n=m÷M=483g÷322g/mol=1.5mol;Na+的物质的量为:2×1.5mol=3mol;所含H2O分子的数目为:1.5mol×10×NA = 15NA。
考点:本题考查物质的量的相关计算。
本题难度:一般