��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
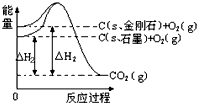
1��ѡ���� ����ͼ��ʾ����H1=��393��5 kJ/mol����H2=��395��4 kJ/mol������˵�����ʾʽ��ȷ����
 [???? ]
[???? ]
A��C��s��ʯī��= C��s�����ʯ�� ��H= +1��9 kJ/mol
B��ʯī�ͽ��ʯ֮���ת���������仯
C�����ʯ���ȶ���ǿ��ʯī
D��1 molʯī���ܼ��ܱ�1 mol���ʯ���ܼ���С1��9 kJ
2������� ���³�ѹ�£�����1mol�����룩������ӻ�ѧ�������յ��������γ�1mol�����룩������ӻ�ѧ�����ų���������Ϊ���ܣ���λΪkJ/mol���±���һЩ�������ݣ�kJ��mol-1��
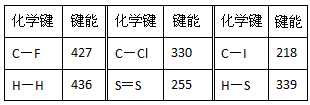
�ش��������⣺
��1���ɱ������ݹ���Ԥ��C��Br���ļ��ܷ�Χ��_________<C��Br����<_________
��2���Ȼ�ѧ����ʽ2H2(g)+S2(g) ==2H2S(g) ��H= QkJ��mol-1����Q=___________
��3����֪�����Ȼ�ѧ����ʽ��
O2(g) == O2+(g) +e- ��H1= +1175��7 kJ��mol-1
PtF6(g) + e-== PtF6-(g) ��H2= -771��1 kJ��mol-1
O2+PtF6-(s) == O2+(g) + PtF6-(g) ��H3= +482��2 kJ��mol -1
��ӦO2(g) +_________(g) = O2+PtF6-(s)�ġ�H=_____________ kJ��mol-1��
3������� ��֪��2SO2��g��+O2��g��
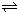
2SO3��g����H=-196.6kJ?mol-1
2NO��g��+O2��g��
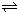
2NO2��g����H=-113.0kJ?mol-1
д��NO2��g����SO2��g������SO3��g����NO��g���Ȼ�ѧ����ʽ______��
��2����֪N2��H2��Ӧ����NH3�������仯��ͼ��ʾ��
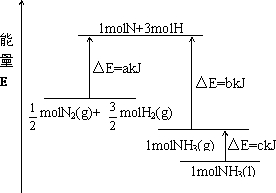
��
1
2
N2(g)+3
2
H2(g)
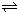
NH3��l������H=______��
4������� ��úת��Ϊˮú������Ҫ��ѧ��ӦΪ��
C+H2O ����
.
CO+H2
C��s����CO��g����H2��g����ȫȼ�յ��Ȼ�ѧ����ʽΪ��
C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
H2��g��+1
2
O2��g���TH2O��g����H=-242.0kJ?mol-1
CO��g��+1
2
O2��g���TCO2��g����H=-283.0kJ?mol-1
��ش�
��1�������������ݣ�д��C��s����ˮ������Ӧ���Ȼ�ѧ��Ӧ����ʽ��______��
��2���ȽϷ�Ӧ�����ݿ�֪��1molCO��g����1molH2��g����ȫȼ�շų�������֮�ͱ�1molC��s����ȫȼ�շų��������࣮��ͬѧ�ݴ���Ϊ��úת��Ϊˮú������ʹúȼ�շų����������������ͬѧ���ݸ�˹������������ѭ��ͼ����ͼ����
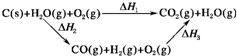
���ݴ���Ϊ��úת��Ϊˮú����ȼ�շų���������úֱ��ȼ�շų���������ȡ���
��������ס�����ͬѧ�۵���ȷ����______����ס����ҡ������жϵ�������______��
��3����úת��Ϊˮú����Ϊȼ�Ϻ�úֱ��ȼ������кܶ��ŵ㣬���о����е������ŵ�______��
______��
��4��ˮú������������������ȼ�ϣ�Ҳ����Ҫ���л�����ԭ�ϣ�
CO��H2��һ�������¿��Ժϳɣ��ټ״����ڼ�ȩ���ۼ��ᡢ�����ᣮ
�Է�����CO��H2��1��1������Ȼ�Ϸ�Ӧ���ϳ�����______������ţ�����ʱ���������㡰��ɫ��ѧ����Ҫ����ȫ����ԭ���е�ԭ�ӣ�ʵ�����ŷţ�
5��ѡ���� ���ݸ�˹�����ж���ͼ��ʾ������ת���������ȷ���ǣ� ? ��
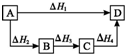 A����H1=��H2=��H3=��H4
B����H1+��H2=��H3+��H4
C����H1+��H2+��H3=��H4
D����H1=��H2+��H3+��H4
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772
|
|
|