微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 白磷(P4)分子呈正四面体结构(如右图所示),科学家受白磷分子的启发,又合成了结构和白磷分子类似的N4分子,下列关于P4和N4分子的说法正确的是

A.P4和N4是同系物
B.P4和N4?是同素异形体
C.P4和N4分子中各原子最外电子层均未达到8电子稳定结构
D.白磷比红磷活泼,N4比N2活泼
参考答案:D
本题解析:略
本题难度:一般
2、选择题 氮族元素随着核电荷数的增加,递变规律正确的是(???)
A.非金属性逐渐增强
B.熔沸点逐渐降低
C.RH3还原性逐渐增强
D.最高价氧化物对应的水化物的酸性逐渐增强
参考答案:C
本题解析:氮族元素从上至下,金属性逐渐增强,非金属性逐渐减弱;单质的熔沸点逐渐升高;氢化物的稳定性逐渐减弱,还原性逐渐增强;而最高价氧化物对应的水化物的酸性逐渐减弱。
本题难度:简单
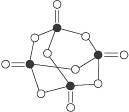
3、选择题 我们平常所说的“五氧化二磷”,其分子组成实为“P4O10”,分子结构呈“笼”状,如图所示(图中●代表磷原子,○代表氧原子)。P4O10极易与水化合,它也可与乙醇、氨等某些具有强极性键的分子结合,反应过程与同水反应类似。每摩尔P4O10与足量的氨反应,最多可消耗氨的物质的量为(???)
A.6 mol
B.8 mol
C.10 mol
D.12 mol
参考答案:D
本题解析:据题意可得,当1 mol P4O10与水化合时,可生成4 mol H3PO4,则同理可得每摩尔P4O10与足量的氨反应需氨12 mol。
本题难度:简单
4、填空题 金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,转化关系如下:
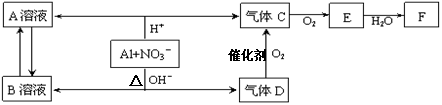
已知,气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。
请回答下列问题:
(1) A和B两溶液混合产生白色沉淀,反应的离子方程式为???????????。
(2) C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,任意写出其中一个反应的化学方程式???????????????????。
(3)写出铝在碱性条件下与NO3-反应的离子方程式?????????????????????????。
(4)除去气体C中的杂质气体E的化学方法:??????????????????(用化学方程式表示)
(5)Al与NO3-在酸性条件下反应,Al与被还原的NO3-的物质的量之比是????????。
参考答案:(1)Al3++3AlO2-+6H2O=4Al(OH)3↓
本题解析:
试题分析:
(1)A和B两溶液混合产生白色沉淀,由信息可知白色沉淀为氢氧化铝。
(2)能转化成无毒的物质,则该物质是氮气。
(3)由流程中的信息铝在碱性条件可以反应得到溶液,所以生成了偏铝酸根。
(4)杂质气体为二氧化氮,除杂时使用水即可。
(5)根据方程式,化合价升降守恒计算可得。
本题难度:一般
5、选择题 砷为第4周期ⅤA元素,根据砷元素在元素周期表中的位置推测,砷不可能具有的性质是( )?
A.砷在通常状况下为固体?
B.As2O3对应水化物的酸性比H3PO4弱?
C.可以有-3、+3、+5等多种化合价?
D.砷的还原性比磷弱?
参考答案:D?
本题解析:同一主族元素,从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,最高价氧化物对应的水化物的酸性减弱。
本题难度:简单