微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 共价键、离子键、分子间作用力等都是构成物质微粒间的不同作用,含有以上所说的两种作用的物质是( )
A.氦
B.石英
C.烧碱
D.食盐
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列哪一组元素的原子间反应可以形成离子键( )
| 原子 | a | b | c | d | e | f | g
M层电子数
1
2
3
4
5
6
7
A.a和c
B.a和f
C.d和g
D.b和g
参考答案:BD
本题解析:
本题难度:简单
3、选择题 下列物质中,含有极性共价键的离子化合物是( )
A.NaOH
B.H2
C.H2S
D.CaCl2
参考答案:A
本题解析:
本题难度:简单
4、填空题 砷化镓广泛用于雷达、电子计算机、人造卫星,宇宙飞船等尖端技术中。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
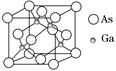
(1)砷化镓的化学式为____________。
(2)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是________(用氢化物分子式表示)。
(3)比较二者的第一电离能:As________(填“<”“>”或“=”)Ga。
(4)下列说法正确的是________(填字母)。
A.砷化镓晶胞结构与NaCl相同
B.砷化镓晶体中与同一个镓原子相连的砷原子构成正四面体
C.电负性:As>Ga
D.砷化镓晶体中含有配位键
参考答案:(1)GaAs (2)NH3>AsH3>PH3 (3)> (
本题解析:由晶胞的结构知每一个砷化镓晶胞中含有4个As原子、4个Ga原子,因此砷化镓的化学式为GaAs。(2)N、P、As为同一主族元素,其氢化物结构相似,相对分子质量越大,则分子间作用力越大,沸点越高,但由于NH3分子间可形成氢键,沸点反常的高,故其氢化物的沸点高低顺序为NH3>AsH3>PH3。(3)As与Ga位于同一周期,分别为ⅤA与ⅢA族,As的p轨道处于半充满的稳定状态,故第一电离能:As>Ga。(4)结合题给GaAs的晶胞结构图可知其晶胞结构与NaCl不同;在GaAs的晶胞中,每个Ga原子连
本题难度:一般
5、选择题 同主族两种元素原子的核外电子数的差值可能是( )
A.6
B.12
C.26
D.30
参考答案:因周期表中1~6周期所含元素种数为2、8、8、18、18、3
本题解析:
本题难度:简单
|