微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏加德罗常数,下列说法错误的是
A.62g白磷(P4)中含P-P键为3NA
B.常温常压下,8.8gCO2和N2O混合物中所含有的分子数为0.2NA
C.25℃时1mL纯水中约含有1×10-10NA个OH-离子
D.标准状况下,22.4L的SO3中含有4NA个原子
参考答案:D
本题解析:分析:A、质量换算物质的量结合1个白磷分子中含6个P-P键分析计算;
B、CO2和N2O摩尔质量都为44g/mol,质量换算物质的量计算分子数;
C、依据水在常温下电离出的氢氧根离子浓度为10-7mol/L,可以看做1L水中氢氧根离子物质的量为10-7mol,1ml水中含氢氧根离子近似为10-10mol,25℃时1mL纯水中约含有1×10-10NA个OH-离子;
D、标准状况三氧化硫不是气体.
解答:A、62g白磷(P4)物质的量=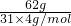 =0.5mol,分子中含P-P键为3NA,故A正确;
=0.5mol,分子中含P-P键为3NA,故A正确;
B、CO2和N2O摩尔质量都为44g/mol,8.8gCO2和N2O物质的量为0.2mol,混合物中所含有的分子数为0.2NA,故B正确;
C、依据水在常温下电离出的氢氧根离子浓度为10-7mol/L,可以看做1L水中氢氧根离子物质的量为10-7mol,1ml水中含氢氧根离子近似为10-10mol,25℃时1mL纯水中约含有1×10-10NA个OH-离子,故C正确;
D、标准状况三氧化硫不是气体;22.4L的SO3物质的量不是1mol,故D错误;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量近似微粒数,化学键的分析判断,水的电离特征应用,气体摩尔体积的条件应用,题目难度中等.
本题难度:简单
2、填空题 已知某种有机物A的质谱图和红外光谱图如下


回答下列问题:
(1)结合以上谱图推断:有机物A的相对分子质量为__________,分子式为__________,有机物A的核磁共振氢谱图中有__________种吸收峰,峰面积之比为__________;该有机物与氢氧化钠溶液在加热条件下反应的化学方程式为:____________________。
(2)直链烃B的相对分子质量比A小4,含2个甲基,并能使溴的四氯化碳溶液褪色,写出B所有可能的结构简式:__________、__________。
(3)链烃C是B的同系物,且其对乙烯的相对密度为3,C的核磁共振氢谱显示:C中只含有一种氢原子。则C在一定条件下发生聚合反应的方程式为:____________________。
参考答案:(1)74;C3H6O2;2;1:1;CH3COOCH3+N
本题解析:
本题难度:一般
3、选择题 2002年诺贝尔化学奖授予瑞士科学家库尔特・芬恩,他的贡献是发明了“利用核磁共振技术测定有机物分子结构”。在有机物分子中,不同的氢原子在质子核磁共振谱中给出的峰值(信号)不同,根据峰值(信号)可以确定有机物分子中氢原子的种类。下列有机物分子中,在质子核磁共振谱中只给出一种峰值(信号) [???? ]
A.CH3OH
B.C(CH3)4
C.CH3COOH
D.CH3COOCH3
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列有机化合物分子中,在氢核磁共振谱中只给出一种信号的是 [???? ]
A. ???????
???????
B.CH3CH2CH3???
C.CH3COOCH3?
D.C(CH3)4
参考答案:D
本题解析:
本题难度:一般
5、选择题 根据下列实验内容得出的结论正确的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A.某物质的水溶液使红色石蕊试纸变蓝,说明溶液呈碱性,可能为碱或水解呈碱性的盐;
B.某气体能使湿润淀粉碘化钾试纸变蓝,说明生成碘,可为氧化性气体;
C.也可能为碳酸氢根离子;
D.计算铁的物质的量,根据反应的方程式计算判断.
解答:A.溶液呈碱性,不一定为碱溶液,可能为水解呈碱性的盐,故A错误;
B.某气体能使湿润淀粉碘化钾试纸变蓝,说明生成碘,可为氧化性气体,不一定为氯气,故B错误;
C.碳酸盐和碳酸氢盐都能与酸反应生成二氧化碳气体,不一定为碳酸根离子,故C错误;
D.n(Fe)=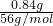 =0.015mol,n(HNO3)=0.05mol,n(Fe):n(HNO3)=0.3,介于0.25~
=0.015mol,n(HNO3)=0.05mol,n(Fe):n(HNO3)=0.3,介于0.25~ 之间,则发生Fe+4HNO3=Fe(NO3)3+NO↑+2H2O和3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,则反应后溶液中一定有Fe3+和Fe2+,故D正确.
之间,则发生Fe+4HNO3=Fe(NO3)3+NO↑+2H2O和3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,则反应后溶液中一定有Fe3+和Fe2+,故D正确.
故选D.
点评:本题综合考查物质的检验、鉴别的实验方案的评价,题目难度中等,注意把握物质的性质,易错点为D,注意把握可能发生的反应与物质的物质的量之间的关系.
本题难度:困难