微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在4FeS2 +11O2== 2Fe2O3+8SO2的反应中,被氧化的元素是
[?????]
A.Fe和S
B.O和Fe
C.S
D.Fe
参考答案:A
本题解析:
解析:
在4FeS2?+11O2== 2Fe2O3+8SO2的反应中,FeS2中的铁元素由+2价变为+3价、硫元素由-1价变为+3价,均被氧化,故A正确,B、C、D错。
故选:A
本题难度:简单
2、填空题 多硫化钠(Na2SX)在制革工业中常用作皮毛的脱毛剂,农业上可作杀虫剂,也是分析化学中的常用试剂。在碱性溶液中,Na2SX与NaBrO3发生反应生成Na2SO4与NaBr。
(1)、上述反应中发生氧化反应的物质是?????????,被还原的元素是??????????????(填写元素符号或化学式)。
(2)、若Na2SX与NaBrO3反应的物质的量之比为3:10,则x = ??????????????????。
(3)、NaBrO3也可以在酸性条件下与NaBr反应生成Br2。若生成6mol Br2,则反应中转移电子的物质的量为?????????????????。
(4)、根据上述两个反应,可推知Na2SX、 Br2、NaBr还原性由强到弱的顺序是????????????(填写化学式)。
参考答案:Na2SX, 本题解析:(1)反应Na2SX+NaBrO3→Na2SO4+NaBr中,溴的化合价由+5价降至―1价,被还原,而硫元素的化合价由负价升到+6价,被氧化
本题解析:(1)反应Na2SX+NaBrO3→Na2SO4+NaBr中,溴的化合价由+5价降至―1价,被还原,而硫元素的化合价由负价升到+6价,被氧化
(2)Na2SX中x个硫原子的化合价共―2价,最终均升为+6价,共升高6x+2价,而NaBrO3中溴的化合价由+5价降至―1价,共降低6价,为升降守恒,两者的物质的量比为3:3x+1,当Na2SX与NaBrO3反应的物质的量之比为3:10,可得x=3
(3)溴元素发生了归中反应:BrO3-+5Br-+6H+=3Br2+3H2O,反应中有5个电子的转移,当
本题难度:简单
3、选择题 某含铬Cr2O72- 废水用硫亚铁铵[FeSO4・(NH4)2 SO4・6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO・FeyCrxO3(Cr为+3价)。不考虑处理过程中的实际损耗,下列叙述错误的是????????????????????(?????)
A.消耗硫酸亚铁铵的物质的量为n(2-x)mol
B.处理废水中Cr2O72- 的物质的量为mol
C.反应中发生转移的电子数为3nx mol
D.在FeO・FeyCrxO3中3x=y
参考答案:A
本题解析:略
本题难度:一般
4、选择题 白磷为剧毒药品,当白磷中毒时可用CuSO4溶液解毒,反应方程式为:P+CuSO4+H2O→Cu3P↓+H3PO4+H2SO4(未配平),当0.5 mol P原子被还原时电子转移总数为(???)
A.3 mol
B.1.5 mol
C.1.806×1024个
D.9.03×1023个
参考答案:C
本题解析:由
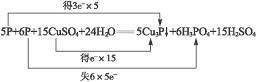
知5 mol P被还原得15 mol e-,转移了30 mol 电子,当0.5 mol P被还原时则转移3 mol e-,即转移电子总数为1.806×1024个,故C正确。
本题难度:简单
5、填空题 高锰酸钾是一种典型的强氧化剂。
完成下列填空:
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO4-+ Cu2S + H+→ Cu2+ + SO2↑ + Mn2+ + H2O(未配平)
② MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O(未配平)
(1)下列关于反应①的说法中错误的是?????????(选填编号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24 L(标况下) SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是: Mn2+> Cu2S
(2)标出反应②中电子转移的方向和数目:?MnO4-+ CuS
Ⅱ.在稀硫酸中,MnO4-和H2O2也能发生氧化还原反应
氧化反应:H2O2-2e → 2H+ + O2↑??????
还原反应:MnO4- + 5e + 8H+ → Mn2+ + 4H2O
(3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为??????????。由上述反应得出的物质氧化性强弱的结论是?????????>___________(填写化学式)。
(4)已知:2KMnO4+ 7H2O2+3H2SO4→ K2SO4+2MnSO4 +6O2↑+10H2O,则被1mol KMnO4氧化的H2O2是
???????mol。
参考答案:(1)d (2分)????????????????????<
本题解析:
试题分析::(1)a.反应中铜元素化合价从+1价升高到+2价,硫元素化合价从-2价升高到+4价,化合价升高的元素被氧化,所以被氧化的元素有S、Cu,故a正确; b.锰元素化合价降低,从+7价降低为+2价,Cu2S元素化合价都升高做还原剂,1molMnO4-得到5mol电子,反应中铜元素化合价从+1价升高到+2价,硫元素化合价从-2价升高到+4价,1molCu2S失去8mol电子,则氧化剂与还原剂的物质的量之比为8:5,故b正确; c.生成2.24LL(标况下)SO2时,物质的量为0.1mol;反应
本题难度:一般