��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��5.6gFe��һ����ϡ������ǡ����ȫ�ܽ������Һ�еμ�NaOH��Һ���������������μ������������ʱֹ���ٽ�������Һ�ͳ���һ��������ɲ��ڿ��������������أ����ù���ɷֺ���������Ϊ
A.A
B.B
C.C
D.D
�ο��𰸣�AB
�������������������5.6gFe��ϡ���ᷴӦ����������������������������������㣬5.6gFe�����ʵ���Ϊ0.1mol�������������ƺ����ɣ��õ�0.1mol���������������������ᱻ������������0.2mol�����ƣ���������0.3mol�����õ�0.05mol��������0.2mol�����ƻ�0.3mol�������ƣ��ɷֱ������������Ƶ�������Χ��
������25.6gFe�����ʵ���=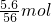 =0.1mol����ȫ��ǡ�����������������������������ʵ���Ϊ0.1mol�������������ƺ����ɣ��õ�0.1mol���������������������ᱻ������������0.2mol�����ƣ�
=0.1mol����ȫ��ǡ�����������������������������ʵ���Ϊ0.1mol�������������ƺ����ɣ��õ�0.1mol���������������������ᱻ������������0.2mol�����ƣ�
����Ԫ�������غ�ɵü�������0.05mol��������0.2mol�������ƣ�
�����ǣ�������0.05mol��160g/mol=8g����������0.2mol��69g/mol=13.8g
���ǡ������������0.1mol������������Ȼ��0.05mol����������0.3mol��
��������������4g������NԪ���غ�ɵ���������0.3mol������Ϊ0.3mol��69g/mol=20.7g
���������������϶���4g��������������Ӧ����[13.8��20.7]�����ڣ�
��ѡAB��
���������⿼������ļ��㣬��Ŀ�ѶȽϴ��⿼��5.6gFe��ϡ���ᷴӦ����������������������������������㣬���ö�ֵ����⣬ע���������������ʱ��������������������������Ϊ�״��㣮
�����Ѷȣ���
2��ѡ���� ij��Һ�д��ڽ϶��H+��SO42����NO3���������Һ�л����ܴ������ڵ���������
A.Mg2+��NH4+��Cl��
B.Mg2+��Ba2+��Br��
C.Na+��Cl����I��
D.Al3+��HCO3����Cl��
�ο��𰸣�A
������������������A�е����ӿ��Ժ���Һ�е�H+��SO42����NO3�����棻B��Ba2+��Һ��SO42���γɳ�����C��Cl����I���ᱻ��Һ�е�����������D�е�HCO3������Һ�е�H+��Ӧ�����ܹ��档
���㣺���ӹ���
�����Ѷȣ���
3��ѡ���� ��һ������NaHCO3������Na2O2�����ϣ��ڼ��������������ַ�Ӧ����Ӧ�����ù���ijɷ�Ϊ
A.Na2CO3
B.Na2CO3��NaOH
C.NaOH
D.Na2CO3��NaOH��Na2O2
�ο��𰸣�A
�������������������ʱ̼�����Ʒֽ����ɶ�����̼��ˮ���ֱ���������Ʒ�Ӧ����̼���ƺ��������ƣ���̼�����ƹ���ʱ�����ɶ�����̼���������ղ���Ϊ̼���ƣ�
��𣺸����漰�Ļ�ѧ����ʽ�У���2NaHCO3 Na2CO3+H2O+CO2������2CO2+2Na2O2�TNa2CO3+O2������2H2O+2Na2O2�T4NaOH+O2������2NaOH+CO2�TNa2CO3+H2O��
Na2CO3+H2O+CO2������2CO2+2Na2O2�TNa2CO3+O2������2H2O+2Na2O2�T4NaOH+O2������2NaOH+CO2�TNa2CO3+H2O��
���������Ʋ��㣬�ڷ�Ӧû����ȫ�������еĹ���ɷ�Ϊ̼���ƣ�
���ڷ�Ӧǡ����ȫ���۷�Ӧδ����ʱ�������еĹ���ɷ���Ϊ̼���ƣ�
���ڷ�Ӧ��ȫ��δ��Ӧ��ȫʱ�������еĹ���ɷ�Ϊ̼���ƺ��������ƣ�
���۷�Ӧ��ȫʱ�������еĹ���ɷ���Ϊ̼���ƺ��������ƣ�
���۷�Ӧ��ȫ������������ʣ��ʱ�������еĹ���ɷ�Ϊ̼���ơ��������ƺ������ƣ�
����й��������������ģ�����̼�����Ʒֽ����ɵĶ�����̼�����������ܺ����������ƣ��������ƺͶ�����̼��Ӧ�����õ��Ĺ���Ϊ̼���ƣ�
��ѡA��
������������Ҫ����ѧ���Ի���������ʵ��������գ��ۺ��Ժ�ǿ���ѶȽϴ�Ҫ��ѧ�����з����ͽ�������������
�����Ѷȣ�һ��
4��ѡ���� �ô�����ʢ��þ�۽���ǿ��ʹ֮ȼ�գ���ַ�Ӧ�����ɵĹ�����������
A.2��
B.3��
C.4��
D.5��
�ο��𰸣�D
���������þ���ڿ�����ȼ��ʱ��þ�۳������������γ�MgO�⣬������N2��CO2��Ӧ����Mg3N2��C��MgO�����ڴ����������ȼ��ʱþ������������е�SiO2��Ӧ����Si��
SiO2+2Mg 2MgO+Si
2MgO+Si
Si��MgҲ���ܷ�Ӧ����Mg2Si��
Si+2Mg Mg2Si
Mg2Si
�ʲ�����5�֣�MgO��Mg3N2��C��Si��Mg2Si����
�����Ѷȣ���
5��ѡ���� ����ͬ�¶��£�������������ʵ���Ũ�ȵ�4��ϡ��Һ����Na2SO4����H2SO3����NaHSO3����Na2S�к����������ɶൽ�ٵ�˳����
A.��=�ܣ���=��
B.��=�٣��ۣ���
C.�ܣ���=�ۣ���
D.�ܣ��٣��ۣ���
�ο��𰸣�D
����������������ȸ���n=CV�������ʵ����ʵ������ٸ������ʵĵ����ˮ������������Ķ��٣�
��𣺵�����������ʵ���Ũ�ȵ�4��ϡ��Һ������n=CV֪�������ʵ����ʵ�����ȣ�
Na2SO4��NaHSO3��Na2S��ǿ����ʣ���ˮ����ȫ���룻Na2SO4��Na2S�������Ӻ������Ӹ�����Ϊ2��1��NaHSO3�������Ӻ������Ӹ�����Ϊ1��1�����������ƺ����Ƶ���Һ����������������������������Һ�е���������������������ǿ��ǿ���Σ���ˮ�в�ˮ�⣬������ǿ�������Σ���ˮ��ˮ�����Һ�д���ɵ��������࣬����������Һ�еĴ�����������������Һ�еĴ�����������������������ʣ�ֻ�в��ֵ��룬������������Һ�д����������٣����Ԣ�Na2SO4����H2SO3����NaHSO3����Na2S�к����������ɶൽ�ٵ�˳���Ǣܣ��٣��ۣ��ڣ�
��ѡD��
���������⿼������Һ�д��������ٵ��жϣ��ѶȽϴ�ע�⣺ǿ�������λ�ǿ��������ˮ���Ե���Ϊ����ˮ�������ģ�
�����Ѷȣ�һ��