微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于下图电化学装置中的电极名称、材料及反应均可能正确的是

A.阴极(Cu片)2C1
参考答案:
本题解析:
本题难度:一般
2、简答题 (12分)
(1)在室温下测得0.1mol・L-1氨水PH=11,则该温度下氨水的电离度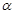 =__________
=__________
(2)25℃时在0.1mol・L-1的H2A水溶液中,用氢氧化钠来调节溶液的pH,得到其中含H2A、HA-、A2-三种微粒的溶液。
①当溶液的pH=7时,c(Na+)=__________(填微粒间量的关系)
②当c(Na+)=c(A2-)+c(HA-)+c(H2A)时溶液为__________溶液(填物质)。
(3)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和液态水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________。
(4)甲醇―空气燃料电池是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:2CH3OH+3O2=2CO2+4H2O。其工作原理示意图如下(其中a、b、c、d四个出入口表示通入或排出的物质)。
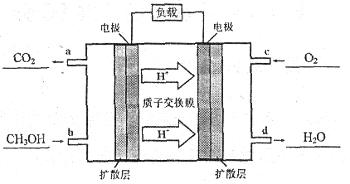
则负极的电极反应式为__________;正极的电极反应式为__________
参考答案:(1)1.0%???(2)① 本题解析:(1)0.1mol・L-1氨水PH=11,则该溶液中OH-浓度是0.001mol/L,所以其电离度是
本题解析:(1)0.1mol・L-1氨水PH=11,则该溶液中OH-浓度是0.001mol/L,所以其电离度是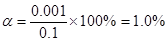 。
。
(2)①根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)可知,当pH=7时,c(Na+)=c(HA-)+2c(A2-)。
②当c(Na+)=c(A2-)+c(HA-
本题难度:一般
3、选择题 试判断下列哪个装置中灯泡会亮
 ?
?
参考答案:C
本题解析:
试题分析:A项:没有形成闭合回路,灯泡不会亮,故错;B、D项:没有氧化还原反应发生,即没有电荷移动,灯泡不会亮,故错。故选C。
点评:记住原电池的形成条件是解题的关键,两个电极、电解质溶液、发生氧化还原反应形成闭合回路。
本题难度:简单
4、填空题 (15分)常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害。某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源
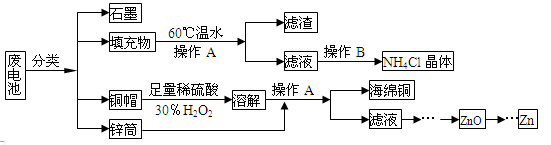
(1)填充物用60℃温水溶解,目的是 。
(2)操作A的名称为 。
(3)铜帽溶解时加入H2O2的目的是 (用化学方程式表示)。
铜帽溶解完全后,可采用_____________方法除去溶液中过量的H2O2。
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为 。
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止。主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4=2MnSO4+4CO2↑+6H2O。
①当1 mol MnO2参加反应时,共有 mol电子发生转移。
②MnO(OH)与浓盐酸在加热条件下也可发生反应,
试写出该反应的化学方程式: 。
参考答案:(15分)
(1)加快溶解速率(2分)
(2)过
本题解析:
试题分析:(1)升高温度,溶解速度加快,所以填充物用60℃温水溶解,目的是:加快溶解速率。
(2)经过操作A得到滤渣和滤液,所以操作A为过滤。
(3)H2O2具有强氧化性,在H2SO4条件下可把Cu氧化为CuSO4,所以化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;H2O2受热分解生成H2O和O2,所以可用加热的方法除去溶液中过量的H2O2。
(4)根据电池总反应,Zn在负极上失电子生成Zn(OH)2,电极方程式为:Zn+2OH--2e-=Zn(OH)2。
(5)①根据化学方程式,当1 mol MnO2参加反应时,同时有2molMnO(OH)反应,Mn元素均转为Mn2+,共有4mol电子发生转移。
②MnO(OH)与浓盐酸的反应可仿照MnO2与浓盐酸的反应,MnO(OH)把HCl氧化为Cl2,配平可得化学方程式:2MnO(OH)+6HCl(浓) 2MnCl2+Cl2↑+4H2O。
2MnCl2+Cl2↑+4H2O。
考点:本题考查化学流程的分析、基本操作、原电池原理、氧化还原反应原理、化学方程式的书写。
本题难度:困难
5、选择题 按如图所示装置进行实验(其中C1、C2均是石墨电极),下列说法中错误的是( )
A.甲池中,Cu极上有气泡放出
B.发现a点附近显红色
C.在C1、C2电极上所产生气体的体积比为2:1
D.乙池溶液的pH减小
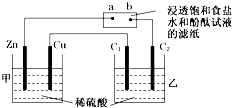
参考答案:A.甲池能自发的进行氧化还原反应,所以属于原电池,锌作负极,
本题解析:
本题难度:一般