微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如下图所示,图I是恒压密闭容器,图Ⅱ是恒容密闭容器。当其他条件相同时,在I、Ⅱ中分别加入2 mol
X和2molY。开始时容器的体积均为VL,发生如下反应并达到平衡状态(提示:物质X、Y的状态均未知,物质Z的状态为气态):2X(?)+Y(?)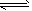 aZ(g) 此时I中X、Y、Z的物质的量之比为1:3:2。下列判断正确的是
aZ(g) 此时I中X、Y、Z的物质的量之比为1:3:2。下列判断正确的是
 [???? ]
[???? ]
A.物质Z的化学计量数a=2
B.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态
C.若X、Y均为气态,则在平衡时X的转化率:I>Ⅱ
D.若X为固态、Y为气态,则I、Ⅱ中从开始到平衡所需的时间:I>Ⅱ
参考答案:BC
本题解析:
本题难度:一般
2、填空题 工业生产硝酸铵的流程图如下:?
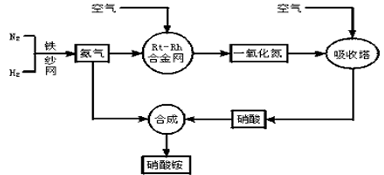
请回答下列问题:
(1)写出硝酸铵在工农业生产中的主要用途____________(任写一条)。
(2)已知N2 (g) +3H2(g) 2NH3(g) △H = -92kJ . mol-1。请回答:
2NH3(g) △H = -92kJ . mol-1。请回答:
①在500℃、200atm和铁催化条件下向一密闭容器中充入 1mol N2和3 mol H2,充分反应后,放出的热量_________(填 “<”“>”或“=”)92.4kJ,理由是_____________。
②为有效提高氢气的转化率,实际生产中宜采取的措施有___________
A.降低温度
B.最适合催化剂活性的适当高温
C.增大压强
D.降低压强
E.循环利用和不断补充氮气
F.及时移出氨
(3)写出氨在铂铑合金网催化氧化下的化学方程式:_________。
(4)在一定温度和压强的密闭容器中,将物质的量之比为 3:2的H2和N2混合,当该反应达到平衡时,测出平衡混合气中氨的体积分数为15%,此时H2的转化率为___________。
参考答案:(1)可做氮肥
(2)①<? ;在latm和2
本题解析:
本题难度:一般
3、选择题 如图是关于N2+3H2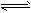 2NH3 ΔH<0的速率-时间图象,则t1时刻使平衡发生移动的原因是
2NH3 ΔH<0的速率-时间图象,则t1时刻使平衡发生移动的原因是
 [???? ]
[???? ]
A.升高温度,同时增大压强
B.降低温度,同时减小压强
C.增大反应物的浓度,同时使用适宜的催化剂
D.增大反应物的浓度,同时减小生成物的浓度
参考答案:D
本题解析:
本题难度:一般
4、填空题 下图是工业生产硝酸铵的流程示意图。
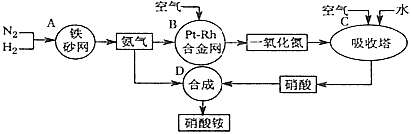
(1)吸收塔C中通入过量空气的目的是______________。A、B、C、D四个容器中的反应,属于氧化还原反应的是_________(填字母)。
(2)已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ;△H= -1266.8kJ/mol
N2(g)+O2(g)=2NO(g);△H= +180.5 kJ/mol
依此写出氨高温催化氧化的热化学方程式:____________________,若上述催化氧化过程转移了5mol电子,则反应的能量变化为_____________。
(3)已知:N2(g)+3H2(g)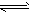 2NH3(g);△H= 一92 kJ/mol。为提高氢气的转化率,宜采取的措施有
2NH3(g);△H= 一92 kJ/mol。为提高氢气的转化率,宜采取的措施有
_________(填字母)。
A.适当升高温度 B.使用更有效的催化剂 C.增大压强
D.循环利用和不断补充氮气 E.及时分离出氨气
(4)在一定温度和压强下,将H2和N2按3∶1(体积比)在密闭容器中混合,当反应达到平衡时,测得平衡混合气中NH3的体积分数为17.6%,此时H2的转化率为___________(计算结果保留一位小数)。
参考答案:(1)使NO充分氧化为NO2;ABC
(2)4NH3(
本题解析:
本题难度:一般
5、选择题 反应:
PCl5(g) PCl3(g)+Cl2(g)①
PCl3(g)+Cl2(g)①
2HI(g)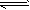 H2(g)+I2(g)②
H2(g)+I2(g)②
2NO2(g)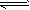 N2O4(g)③
N2O4(g)③
在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各反应的温度和容器的体积都不改变,分别再加入一定量的各自的反应物,则转化率
[???? ]
A.均不变
B.均增大
C.①增大,②不变,③减少
D.①减少,②不变,③增大
参考答案:D
本题解析:
本题难度:一般
来源:91考试网 91Exam.org