微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中,有关离子一定能大量共存的是(??? )
A.能使石蕊呈红色的溶液中: Na+、I-、Cl-、NO3-
B.能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO-
C.能使pH试纸变红色的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+
D.无色溶液中:K+、Cl-、NO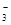 、SO
、SO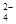
参考答案:D
本题解析:A.能使石蕊呈红色的溶液呈酸性,其中的NO3-具有强氧化性,可与还原性较强的I-发生氧化还原反应
B.溶液中的ClO-具有强氧化性,可与具有强还原性的SO32-离子发生氧化还原反应
C.能使pH试纸变红色的溶液呈酸性,[Ag(NH3)2]+不可能大量存在:[Ag(NH3)2]++2H+=Ag++2NH4+
D.可以大量共存,答案为D
本题难度:一般
2、选择题 关于氯化铁水解的说法错误的是????????????????????????( )
A.水解达到平衡(不饱和)时,无论加氯化铁饱和溶液还是加水稀释,平衡均向正方向移动
B.浓度为5 mol/L和0.5 mol/L的两种FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者小
C.有50℃和20℃的同浓度的FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者小
D.为抑制Fe3+水解,较好地保存FeCl3溶液,应加少量盐酸
参考答案:B
本题解析:略
本题难度:简单
3、选择题 下列说法中正确的是
A.常温下水电离出c(H+)×c(OH-)=10-20的溶液中:Na+、ClO-、SO42-、NH4+能大量共存
B.常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存
C.一定温度下。l L 0.5 mol・L-1NH4C1溶液与2 L 0.25 mol・L-1NH4Cl溶液含NH4+物质的量相同
D.反应ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq)说明Ksp(ZnS)>Ksp(CuS)
参考答案:D
本题解析:
试题分析:A、常温下水电离出c(H+)×c(OH-)=10-20的溶液,说明溶液可能是酸性也可能是碱性,ClO-在酸性条件和H+反应生成弱酸HClO不共存,NH4+在碱性条件:NH4++OH-=NH3・H2O不共存,错误;B、在离子组中,Fe3+不能在pH=7溶液中存在,转变成Fe(OH)3,错误;C、NH4Cl是强酸弱碱盐,NH4+水解:NH4++H2O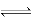 NH3・H2O+H+,浓度越小,越促进水解,0.5mol・L-1NH4Cl中c(NH4+)最大,错误;D、Ksp的应用,同一类型的Ksp越小,说明该物质越难溶,同时反应向着更难溶的方向进行,Ksp(ZnS)>Ksp(CuS),正确。
NH3・H2O+H+,浓度越小,越促进水解,0.5mol・L-1NH4Cl中c(NH4+)最大,错误;D、Ksp的应用,同一类型的Ksp越小,说明该物质越难溶,同时反应向着更难溶的方向进行,Ksp(ZnS)>Ksp(CuS),正确。
考点:考查盐类水解、溶度积、影响水电离的因素等相关知识。
本题难度:一般
4、选择题 在下列无色透明溶液中,能大量共存的离子组是(?)
A.Fe2+、Na+、SO42-、Cl-
B.K+、Na+、HCO3-、NO3-
C.OH-、HCO3-、Ca2+、Na+
D.Mg2+、Na+、OH-、NO3-
参考答案:B
本题解析:
试题分析:A项:Fe2+呈绿色,故错;C项:OH-和HCO3-反应不能共存,故错;D项:Mg2+和OH-反应生成白色沉淀不能共存,故错。故选B。
点评:解答离子共存问题时,学生们需注意以下几点:(1)离子间相互结合形成沉淀、气体、弱电解质、络离子时不能大量共存;离子间发生双水解反应、氧化还原反应时不能大量共存。(2)注意题目的限制条件。
本题难度:一般
5、选择题 下列各组离子能在强碱性溶液中大量共存的是( )
A.K+、Na+、SO42-、NO3-
B.H+、Na+、Cl-、SO42-
C.Cu2+、K+、Cl-、SO42-
D.K+、NH4+、HCO3-、Cl-
参考答案:A.在碱性条件下,离子之间不发生任何反应,可大量共存,故A正
本题解析:
本题难度:简单