��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���ݵ��ܱ������г���0.1 mol/L CO2��0.1 mol/L CH4����һ�������·�����Ӧ��CH4(g)��CO2(g)  2CO(g)��2H2(g)�����CH4ƽ��ʱת�������¶ȡ�ѹǿ��ϵ��ͼ�������й�˵������ȷ����
2CO(g)��2H2(g)�����CH4ƽ��ʱת�������¶ȡ�ѹǿ��ϵ��ͼ�������й�˵������ȷ����
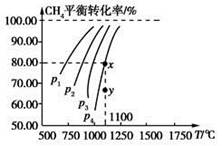
A��������Ӧ�Ħ�H<0
B��ѹǿ��p4>p3>p2>p1
C��1100 ��ʱ�÷�Ӧƽ�ⳣ��Ϊ1.64
D��ѹǿΪp4ʱ����y�㣺v��>v��
�ο��𰸣�A
������������⿼���˻�ѧƽ�⣬���ڿ��鿼���Ի�ѧƽ���ƶ�ԭ�������⼰������������ͼ���֪��ѹǿһ��ʱ���¶�Խ�ߣ������ƽ��ת����Խ�ߣ�������ӦΪ���ȷ�Ӧ����H>0��A����÷�ӦΪ������������ӵķ�Ӧ��ѹǿԽ�ߣ������ƽ��ת����ԽС����ѹǿp4>p3>p2>p1��B����ȷ��1100 ��ʱ�������ƽ��ת����Ϊ80.00%����ƽ��ʱ�����ʵ�Ũ�ȷֱ�Ϊc(CH4)��0.02 mol/L��c(CO2)��0.02 mol��c(CO)��0.16 mol/L��c(H2)��0.16 mol/L����ƽ�ⳣ��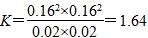 ��C����ȷ��ѹǿΪp4ʱ��y��δ�ﵽƽ�⣬��ʱv��>v�棬D����ȷ��
��C����ȷ��ѹǿΪp4ʱ��y��δ�ﵽƽ�⣬��ʱv��>v�棬D����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ��һ�������·�����Ӧ 2A(g) === 2B(g)+C(g)����2 mol Aͨ��2 L�ݻ��㶨���ܱ��������У���ά���������¶Ȳ��䣬5 minĩ���A�����ʵ���Ϊ0.8 mol����B��Ũ�ȱ仯����ʾ�÷�Ӧ������Ϊ [???? ]
A��0.24 mol/(L��min)
B��0.08 mol/(L��min)
C��0.06 mol/(L��min)
D��0.12 mol/(L��min)
�ο��𰸣�D
���������
�����Ѷȣ���
3��ѡ���� �����������з�����ͬ�ķ�Ӧ�� A(g) + 3B(g) 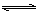 2C(g) �����ݡ��Һ�ѹ���¶���ͬ���㶨����ʼʱ���м���0.01mol A��0.03mol B�����м���0.02molC����ʼʱ������ѹǿ��ȣ����ֱ�ﵽƽ�⡣�����й�����ƽ��״̬��������ȷ����(? )
2C(g) �����ݡ��Һ�ѹ���¶���ͬ���㶨����ʼʱ���м���0.01mol A��0.03mol B�����м���0.02molC����ʼʱ������ѹǿ��ȣ����ֱ�ﵽƽ�⡣�����й�����ƽ��״̬��������ȷ����(? )
A�����������С����????????? B��C�����ʵ�������һ��С����
C��ѹǿ�����ܴ�����????????? D��A��CŨ�ȱ�ֵc(A)/c(C)����һ��С����
�ο��𰸣�B
�����������
�����Ѷȣ���
4�������� ��3 mol A��2.5 mol B�����2L���ܱ������У�������Ӧ�Ļ�ѧ����ʽΪ��3A(��) + B(��)  ?xC(��) + 2D(��)��5 min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ�ٶ�Ϊ 0.1 mol/(L�qmin), ��д���пհף�
?xC(��) + 2D(��)��5 min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ�ٶ�Ϊ 0.1 mol/(L�qmin), ��д���пհף�
(1) x =______
(2) ƽ��ʱC��Ũ��Ϊ ________________
(3) ƽ��ʱB��ת����Ϊ _____________
(4) ƽ��ʱ�������ڵ�ѹǿ��ԭ������ѹǿ�ı�ֵΪ ___________
�ο��𰸣�(1)X="1" ????(2) 0.25mol��L-1??
��������������ڵ�ѹǿ��С��˵��3+1��x+2������Ϊx������������x��1��D��ƽ����Ӧ�ٶ�Ϊ 0.1 mol/(L�qmin),��������D��0.1 mol/(L�qmin),��2L��5min��1.0mol
3A(��) + B(��)  ?C(��) + 2D(��)
?C(��) + 2D(��)
��ʼ����mol��?? 3????? 2.5?????????? 0???? 0
ת������mol��?? 1.5??? 0.5?????????? 0.5??? 1.0
ƽ������mol��?? 1.5??? 2.0?????????? 0.5??? 1.0
����ƽ��ʱC��Ũ��Ϊ0.5mol��2L��0.25mol/L
ƽ��ʱB��ת����Ϊ0.5��2.5��100����20��
��Ϊѹǿ֮�������ʵ�����֮��
����ƽ��ʱ�������ڵ�ѹǿ��ԭ������ѹǿ�ı�ֵΪ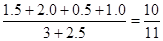
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ʾΪ8000CʱA��B��C�����������ܱ������з�ӦʱŨ�ȵı仯��ֻ��ͼ�Ϸ������ܵó��Ľ����ǣ�??��?
 ?
?
A��A�Ƿ�Ӧ��?
B��ǰ2 min A�ķֽ�����Ϊ0.1mol?L-1?min-1?????????????
C����ƽ����������¶ȣ�ƽ��������Ӧ�����ƶ�?
D����ƽ���������ѹǿ��ƽ�����淴Ӧ�����ƶ�????????????
�ο��𰸣�C
�������������A��Ũ���Ǽ�С�ģ������Ƿ�Ӧ�ѡ��A��ȷ��ǰ2 min A��Ũ�ȱ仯��0.2mol/L�������䷴Ӧ������0.1mol?L-1?min-1��ѡ��B��ȷ�����ڲ���ȷ����Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ������ѡ��C����ȷ�����������ʵı仯����֪����Ӧ�ķ���ʽ��2A 2B��C��������Ӧ���������ģ���������ѹǿ��ƽ�����淴Ӧ�����ƶ���ѡ��D��ȷ����ѡC��
2B��C��������Ӧ���������ģ���������ѹǿ��ƽ�����淴Ӧ�����ƶ���ѡ��D��ȷ����ѡC��
�����Ѷȣ���