微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Na2SO3是常用的抗氧剂。
(1)实验室通常用浓硫酸(1:1)和Na2SO3微热制备SO2气体,
反应方程式为:??????????????????????????????,制备的SO2气体中通常含有水蒸气,下列干燥剂能干燥SO2气体的是:????????????;
A.浓硫酸???? B.碱石灰???? C.无水CaCl2???
(2) 少量SO2气体通入NaOH溶液中可得NaOH和Na2SO3的混合溶液,向该混合溶液中加入少许溴水,振荡后溶液变为无色。碱性溶液中Br2与Na2SO3发生氧化还原反应,反应的离子方程式为______________;
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告;
限选试剂:2 mol・L-1HCl;1 mol・L-1H2SO4;1mol・L-1HNO3;1 mol・L-1BaCl2;
1 mol・L-1Ba(NO3)2;0.1 mol・L-1AgNO3;CCl4;苯;新制饱和溴水;新制饱和氯水。
编号
| 实验操作
| 预期现象和结论
|
步骤①
| 取少量待测液于试管A中,滴加2 mol・L-1HCl至溶液呈酸性,加入几滴________(填试剂),振荡
| ________,证明待测液中含SO32-
|
步骤②
| 另取少量待测液于试管B中,加入????????????,再滴加适量
1 mol・L-1 BaCl2溶液
| ????????????????????
???????????????????
|
步骤③
| 另取少量待测液于试管C中,????????????????????????,振荡,静置后观察颜色
| 溶液分层,上层液体呈橙红色,证明待测液中很Br-
?
参考答案:(1) 本题解析: 本题解析:
试题分析:(1)根据强酸制弱酸,浓硫酸(1:1)和Na2SO3微热可制取SO2,化学方程式为: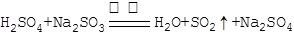 ;SO2为酸性氧化物,不能用碱石灰干燥,可用浓硫酸或无水CaCl2干燥,故A、C项正确。 ;SO2为酸性氧化物,不能用碱石灰干燥,可用浓硫酸或无水CaCl2干燥,故A、C项正确。
(2)Br2把Na2SO3氧化为SO42?,在碱性条件下离子方程式为:SO32-+Br2+2OH-=H2O+SO4
本题难度:困难
2、选择题 臭氧(O3)可使湿润的KI淀粉试纸变蓝,反应为KI+O3+H2O KOH+I2+O2(未配平),由此可得出下列结论正确的是( )? KOH+I2+O2(未配平),由此可得出下列结论正确的是( )?
A.O3在反应中被氧化为O2?
B.O3的氧化能力大于O2?
C.1 mol O3在反应中得到2 mol电子?
D.反应中氧化产物O2与还原产物I2的物质的量之比为1∶1
参考答案:C
本题解析:反应配平后:2KI+O3+H2O====2KOH+I2+O2
还原剂为I-,氧化剂为O3中的1个氧原子。
A中说O3在反应中被氧化,是错误的。
B中O3比O2的氧化能力大的说法是正确的,如Ag、Hg在空气或氧气中不易被氧化的金属,可以与臭氧发生反应。但在本题中由于O2的化合价没有改变,它既不是氧化产物也不是还原产物,故得出O3的氧化能力大于O2是不正确的。C项正确。D项不正确,O2不是氧化产物。
本题难度:简单
3、填空题 煤是一种常用的燃料。由于煤燃烧产生的废气中含有SO2、NO2和NO等多种有害气体和烟尘,会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放。
(1)将煤直接进行燃烧,造成环境污染的主要原因之一是形成硝酸型酸雨。
①写出有关物质转化为硝酸的化学方程式____________________________。
②以下是对硝酸型酸雨的评价,其中正确的是_________________________(用序号填空)。
a.杀死水中的浮游生物,减少鱼类食物来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.破坏臭氧层
d.硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥
(2)如图是对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图,试写出在废气脱硫并形成副产物的过程中所发生的主要化学反应的化学方程式_______。
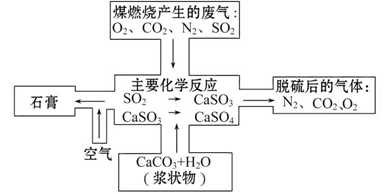
(3)脱硫以后,在废气中含量明显增加的不良气体是(写物质名称)_______,它对环境的负面影响是____________________________________________。
(4)检验脱硫后废气中是否含有SO2的简单方法是_________________________。
参考答案:(1)①2NO+O2=2NO2,
3NO2+H2O=2
本题解析:(1)形成硝酸型酸雨,这说明煤燃烧生成了NO和NO2等氮氧化物,NO跟O2反应生成NO2,NO2跟H2O反应生成HNO3。硝酸型酸雨有它的危害性,但它所含有的氮元素又是植物所需要的主要元素之一。因此应该一分为二地评价酸雨的利与弊。这里不是对NO和NO2的评价,而是对硝酸型酸雨的评价,该酸雨对臭氧层没有破坏作用。
(2)由图可知,脱硫是硫元素转化为CaSO4,最终产品是石膏CaSO4・2H2O。
(3)通过问题(2)的解答可知,在脱硫的同时生成了CO2,并且CO2与SO2以等物质的量代换。
本题难度:一般
4、选择题 下列几种物质均能使品红褪色,其中有一种物质使品红褪色的原理与其他几种不同,该物质是(???)
A.过氧化钠
B.臭氧
C.二氧化硫
D.过氧化氢
参考答案:C
本题解析:选项ABD都是强氧化性导致褪色,SO2是和有色物质化合生成不稳定的无色物质,所以答案选C。
本题难度:一般
5、选择题 某浓H2SO4的标签上写明含H2SO4 96~98.3%,欲得其准确的值,有效的方法是
A.测pH值
B.测导电性大小
C.测密度
D.进行中和滴定
参考答案:CD
本题解析:
试题分析:要获得浓硫酸质量分数的准确的值,根据质量分数= ×100%可知,需要获得一定体积浓硫酸溶液的质量与溶质的质量,据此结合选项解答。A、测pH值,只能获得溶液中氢离子的浓度,浓硫酸中硫酸主要以分子形式存在,不能确定硫酸的物质的量浓度,A不正确;B、测导电性大小,只能获得溶液中离子的浓度,浓硫酸中硫酸 ×100%可知,需要获得一定体积浓硫酸溶液的质量与溶质的质量,据此结合选项解答。A、测pH值,只能获得溶液中氢离子的浓度,浓硫酸中硫酸主要以分子形式存在,不能确定硫酸的物质的量浓度,A不正确;B、测导电性大小,只能获得溶液中离子的浓度,浓硫酸中硫酸
本题难度:一般
|