��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������У�������ԭ�ӻ�����������㶼Ϊ8���ӽṹ���� [???? ]
A��HCl
B��Na2S
C��LiCl
D��H2O
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� ���б�ʾ���ʵĻ�ѧ������ȷ���ǣ�������
A��NH4H�ĵ���ʽ��
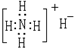
B���������Ľṹ��ʽ��
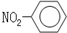
C�������ǵ�ʵ��ʽ��CH2O
D��������ӵı���ģ�ͣ�
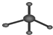
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� A��B��C���ֶ�����Ԫ����Ԫ�����ڱ��е�λ����ͼ��ʾ����֪A��CԪ�ؿɷֱ���BԪ���γɻ�����X��Y��A��B��������֮�͵���C������������������˵���������ж���ȷ������ǣ�������
| A | B
C
��B��C������ͬ��������
��X�������Y�Ķ�
�۷е㣺A������⻯�����C������⻯��
��C������������Ӧˮ��������A���⻯���γ������Σ�
A���٢ڢۢ�
B���ڢ�
C���٢ڢ�
D���٢�
�ο��𰸣�A��B��C���ֶ�����Ԫ�أ���A��������Ϊx������ͼ��֪��C��
���������
�����Ѷȣ�һ��
4������� A��B��C��D��E��Ϊ������Ԫ�أ��仯�ϼ���ԭ�������Ĺ�ϵ����ͼ��ʾ��
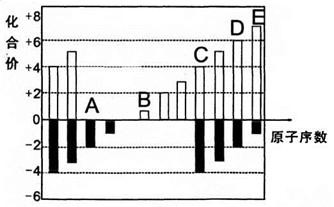
(1)A��B��C��D����Ԫ���е�һ��������С����???(��Ԫ������)�����̬ԭ�Ӻ�������Ų�ʽ��???��
(2)D��E������������ˮ�����У����Խ�ǿ����???????(д��ѧʽ)��
D���⻯��е��A���⻯��е�?????(��ߡ��͡�)��
(3)������CA2�ľ���������______��CA2��B���{���������ˮ������Һ������Ӧ�����ӷ���ʽ��_______
(4)��298K��101.3kPa�£�1.6gD������������������ȼ�գ��ų�14.85kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��______________
�ο��𰸣�����16�֣�
��1���ƣ�2�֣�???? 1s22s22
���������
����������л��ϼۿ�����֪A��B��C��D��E�ֱ�ΪO��Na��Si��S��Cl��
��1��������Խǿ��Խ��ʧ���ӣ���һ������ԽС����Na��С��
��2���ǽ�����Խǿ������������Ӧˮ����ļ���Խǿ���ǽ���Cl>S��H2O����������ʷе�ϸߣ�
��3��SiO2Ϊԭ�Ӿ��壬Ϊ���������������ǿ�����Ӧ��
��4��1.6gS�����ʵ���Ϊ0.05mol����1molS��Ӧ�ų�������Ϊ14.85KJ/0.05mol=297.0KJ/mol���Ӷ�д���Ȼ�ѧ����ʽ��
�����Ѷȣ�һ��
5��ѡ���� �ü۵��ӶԻ�������Ԥ��H2S��BF3�Ŀռ乹�ͣ��������۶���ȷ����(����)
A��ֱ���Σ�������
B��V��������
C��ֱ���Σ�ƽ��������
D��V�Σ�ƽ��������
�ο��𰸣�D
���������
��D���۵��ӶԻ�������Ԥ�⣬H2S��BF3�ֱ����sp3��sp2�ӻ���H2S�����Թµ��Ӷԣ��ռ乹�ͣ�BF3�ռ乹��Ϊƽ����������
�����Ѷȣ���
|