��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ����
[???? ]
A���κη�Ӧ�е������仯������Ϊ�����仯
B�����ʷ�����ѧ�仯�������������仯
C�����������仯�����ʱ仯���ǻ�ѧ�仯
D����ʹû�����ʵı仯��Ҳ�����������ı仯
�ο��𰸣�B
���������
�����Ѷȣ���
2������� ��14�֣���֪��NaAlO2�Ʊ�����Al(OH)3������ת����ϵ��ͼ��
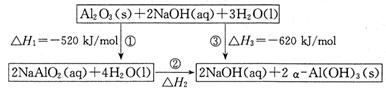
��1����Ӧ�ڵ��Ȼ�ѧ����ʽΪ??????????????????????????��
��2��������������ת����ϵ���ݶ���˾�ҵ���һ�ּ�ݵĴ��������ȡAl2O3�ķ������������£�

������A�Ļ�ѧʽΪ???????????��
�ڲ����Ļ�ѧ��Ӧ����ʽΪ????????????????????????????????????�����鲽����г����Ƿ�ϴ���ķ�����??????????????????????????��
�۲���������ȴ�ķ�����������Al(OH)3���ô�ʩ��������???????????????��
�ܹ�ҵ�Ͽɵ����������Al2O3�Ի��Al�������2.7kgAl��������������A�����ʵ�������Ϊ???????mol���������������Na[AlCl4]��NaCl�Ļ�������Al2O3���е����Al����������ӦΪ??????????????��
�ο��𰸣���14�֣�
��1��NaAlO2(aq)+2H2O(l)
���������
�����������1������д����Ӧ�ڵĻ�ѧ����ʽ��ע��״̬NaAlO2(aq)+2H2O(l) = NaOH(aq)+����Al(OH)3��s�����ݸ�˹��������÷�Ӧ���ʱ�?H=?��1/2?H1 + 1/2?H3=��50kJ?mol?1���ɵ��Ȼ�ѧ����ʽΪ��
��2����Al2O3Ϊ�����������������AΪNaOH��
�ڲ����ΪAl(OH)3���շֽ�����Al2O3�����Ի�ѧ����ʽΪ��2Al(OH)3 �����Ѷȣ�һ��
�����Ѷȣ�һ��
3��ѡ���� ��֪�Ȼ�ѧ����ʽ��SO2(g)+ 1/2O2(g)  ?SO3(g) ��H= �D98.32kJ��mol���������г���2molSO2��1molO2��ַ�Ӧ�����շų�������Ϊ?????��?��
?SO3(g) ��H= �D98.32kJ��mol���������г���2molSO2��1molO2��ַ�Ӧ�����շų�������Ϊ?????��?��
A��196.64kJ
B��196.64kJ��mol
C����196.64kJ
D����196.64kJ
�ο��𰸣�C
�����������
�����Ѷȣ���
4��ʵ���� ijʵ��С����0.50 mol��L-1NaOH��Һ��0.50 mol��L-1������Һ�����к��ȵIJⶨ��
��.����0.50 mol��L-1NaOH��Һ
(1)��ʵ���д�ԼҪʹ��470 mL NaOH��Һ,������Ҫ����NaOH������������g��?
(2)��ͼ��ѡ�����NaOH��������Ҫ��������(����ĸ):����������?
����
| ������ƽ
(������)
| С�ձ�
| ����ǯ
| ������
| ҩ��
| ��Ͳ
|
����
| 
| 
| 
| 
| 
| 
|
���
| a
| b
| c
| d
| e
| f
?
��.�ⶨ�к���
(1)ʵ�����ϱ����ձ�(��С�����ձ�)����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����ᡢNaOH��Һ,��ȱ�ٵ�ʵ�鲣����Ʒ������������?
(2)ȡ50 mL NaOH��Һ��30 mL������Һ����ʵ��,ʵ���������±���
������д�±��еĿհ�:
ʵ��
����
| ��ʼ�¶�t1/��
| ��ֹ�¶�
t2/��
| �¶Ȳ�ƽ��ֵ
(t2-t1)/��
| H2SO4
| NaOH
| ƽ��ֵ
| 1
| 26.2
| 26.0
| 26.1
| 30.1
| ?
| ?
| 2
| 27.0
| 27.4
| 27.2
| 33.3
| ?
| 3
| 25.9
| 25.9
| 25.9
| 29.8
| ?
| 4
| 26.4
| 26.2
| 26.3
| 30.4
| ?
?
�ڽ�����Ϊ0.50 mol��L-1NaOH��Һ��0.50 mol/L������Һ���ܶȶ���1 g/cm3,�кͺ�������Һ�ı�����c=��4.18��J/(g����)�����к��Ȧ�H=������������(ȡС�����һλ)��?
������ʵ����ֵ�����57.3 kJ��mol-1��ƫ��,����ƫ���ԭ�������(����ĸ)����������?
A.ʵ��װ�ñ��¡�����Ч����
B.��ȡNaOH��Һ�����ʱ���Ӷ���
C.�ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
D.���¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
�ο��𰸣���.(1)10.0��(2)abe
��.(1)�������
�������������һ�����ʵ���Ũ����Һ�����ơ��к��ȵIJⶨ�Լ���������
��.(1)����û��470 mL������ƿ,����Ӧ������500 mL 0.50 mol��L-1NaOH��Һ��������Ҫ�������Ƶ�������500 mL��10-3��0.5 mol/L��40 g/mol="10.0" g��
(2)�������ƾ��и�ʴ�Ժ���ˮ��,����Ӧ�÷����ձ��г���,ͬʱ����Ҫҩ��ȡNaOH����,������ȷ�Ĵ�ѡabe��
��.(1)���к��ȵIJⶨʵ����,��Һ����Ҫ�����,���Ի�ȱ�ٻ��β����������
(2)���Ĵ�ʵ����¶Ȳ�
�����Ѷȣ�һ��
5��ѡ���� ��֪��Ӧ����101kPaʱ��C(s) �� 1/2O2(g)��CO��g������H1����110.5kJ/mol
��������������ϡ��Һ�У�H+(aq) �� OH-(aq)��H2O(1)����H2����57.3kJ/mol
���н�����ȷ����
A����̼��ȼ�����á�H3����ʾ�����H3<��H1
B����̼��ȼ�����á�H3����ʾ�����H3>��H1��
C��Ũ������ϡNaOH��Һ��Ӧ����1molˮ���ų�57.3kJ����
D��ϡ������ϡNaOH��Һ��Ӧ����1molˮ���ų�57.3kJ����
�ο��𰸣�A
���������
���������ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ų���������1mol̼��ȫȼ�����ɶ�����̼�ų�������������һ����̼�ų������࣬�O��H3�O>�O��H1�O��A��ȷ���к�����ָϡ��Һ��ǿ���ǿ������1molH2O�ų���������C��Ũ��������ˮҲҪ�ų�������D�д��������Ҫ����������
������ȷ����ȼ���Ⱥ��к��ȵĸ��
�����Ѷȣ�һ��
|
|