微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 将一定量的SO2和含0.7 mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2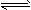 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数) 请回答下列问题:
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数) 请回答下列问题:
(1)判断该反应达到平衡状态的标志是__________。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)求该反应达到平衡时SO2的转化率(用百分数表示)。
(3)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?
2、填空题 肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料。请回答下列问题
(1)直接肼燃料电池原理如图所示,通入N2H4的极为电池的__________极。(填:正、负)
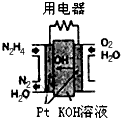
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H=-67.7kJ・mol-1,
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ・mol-1
2NO2(g)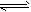 N2O4(g) △H=-52.7kJ・mol-1
N2O4(g) △H=-52.7kJ・mol-1
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:_____________________。
(3)肼的水合物(水合肼,N2H4・2H2O)是一种强还原剂,某文献报道用Fe-Al复合催化剂催化水合肼可选择性还原对氯硝基苯制备对氯苯胺,某次实验部分记录如下

请分别从实验Ⅰ、Ⅱ、Ⅲ组合出最佳条件依次为_________________(选用序号①②③④⑤)。
(4)已知:2NO2(g)==N2O4(g) △H=-57.20kJ・mol-1。一定温度下,在密闭容器中反应
2NO2(g)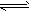 N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是__________(填字母)
N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是__________(填字母)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(5)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol・L-1、
c(N2O4)=0.0120 mol・L-1。计算反应2NO2(g) N2O4(g)的平衡常数K。
N2O4(g)的平衡常数K。
_______________________________
3、填空题 在容积为2L的密闭容器中,保持体系内温度为800℃不变,将一定量的X和Y气体混合发生反应:
2X(g)+Y(g)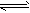 2Z(g) 其中X的物质的量[n(X)]随时间的变化如下表
2Z(g) 其中X的物质的量[n(X)]随时间的变化如下表
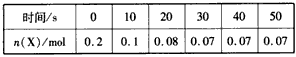
请回答下列问题:
(1)用Y表示反应开始至达到平衡(假设30s刚刚达到平衡)时的平均反应速率__________,0~10s与10~20 s的反应速率之比为___________。
(2)根据上述数据,能否计算800℃时该反应的平衡常数K,“能”则计算K=____________;“否”则说明缺少的数据:____________。
(3)若升高反应体系的温度,使反应重新达到平衡,此时体系中n(X)=n(Z),则该反应是__________(选填 “吸”、“放”)热反应。
(4)在800℃时,若缩小容器的体积,达到新平衡时n(X)___(选填“>”、“=”或“<”)0.07 mol,X的转化率_______(选填“增大”、“不变”或“减小”)。
(5)上述800℃时的反应达到平衡时测得放出热量akJ。试写出在此条件下X与Y反应的热化学方程式___________________________。
4、选择题 对于可逆反应A(g)+2B(g) 2C(g)( △H>0),下列图象中正确的是 [???? ]
2C(g)( △H>0),下列图象中正确的是 [???? ]
A.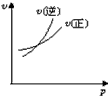
B.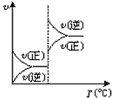
C.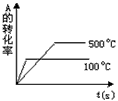
D.
5、选择题 在密闭的容器中进行如下反应:H2(g)+I2(g)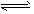 2HI(g),在温度T1和T时,产物的量和时间的关系如图所示,根据图象判断正确的是
2HI(g),在温度T1和T时,产物的量和时间的关系如图所示,根据图象判断正确的是
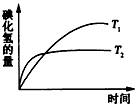 [???? ]
[???? ]
A. T1< T2 ,△H<0
B. T1> T2 ,△H<0
C. T1<T2 ,△H>0?
D. T1>T2 ,△H>0