微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式书写正确的是
A.碳酸钙溶于稀硝酸:CaCO3+2H+═Ca2++CO2↑+H2O
B.氯化亚铁溶液中加入NaHS溶液:Fe2++HS-═FeS↓+H+
C.碳酸钠稀溶液中通入二氧化碳:CO32-+CO2+H2O═2HCO3-
D.硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH--═NH3↑+H2O
参考答案:AC
本题解析:分析:A.反应生成硝酸钙、水、二氧化碳;
B.不发生化学反应,FeS能与HCl反应;
C.反应生成碳酸氢钠;
D.加入少量氢氧化钠溶液,只发生氢离子与碱的反应.
解答:A.碳酸钙溶于稀硝酸的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故A正确;
B.氯化亚铁溶液中加入NaHS溶液,不发生反应,则不存在离 子反应,故B错误;
C.碳酸钠稀溶液中通入二氧化碳的离子反应为CO32-+CO2+H2O═2HCO3-,故C正确;
D.硫酸氢铵溶液中加入少量氢氧化钠溶液的离子反应为H++OH--═H2O,故D错误;
故选AC.
点评:本题考查离子反应方程式书写的正误判断,明确发生的化学反应是解答本题的关键,题目难度中等,选项B为解答的易错点.
本题难度:一般
2、选择题 下列物质中,既能跟盐酸反应又能跟氢氧化钠溶液反应的是
A.Al(OH)3
B.NaAlO2
C.AlCl3
D.Fe
参考答案:A
本题解析:分析:根据物质间的反应进行判断,中学常见的既能与酸反应又能与碱反应的物质主要有:
①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;
②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;
③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;
④某些具有两性的金属:Zn、Al等;
⑤某些非金属:Si、S等;
⑥其它一些物质.如:a、某些盐类物质既与酸反应,又与碱反应;
b、个别酸性氧化物SiO2;
c、具有还原性的无氧酸:H2S、HI等与氧化性酸反应、与碱反应;
d、具有氧化性酸:浓H2SO4、HNO3等与还原性酸反应、与碱反应,以此解答本题.
解答:A.氢氧化铝是两性氢氧化物,能与盐酸反应生成氯化铝与水,与氢氧化钠反应生成偏铝酸钠与水,故A符合;
B.NaAlO2与盐酸反应生成氯化铝,与氢氧化钠不反应,故B不符合;
C.AlCl3能与氢氧化钠溶液反应生成氢氧化铝或偏铝酸钠,不与盐酸反应,故C不符合;
D.Fe只能与盐酸反应生成氯化亚铁与氢气,不能与氢氧化钠溶液反应,故D不符合;
故选A.
点评:本题考查了物质的性质,难度不大,旨在考查学生对知识的理解识记与知识归纳,明确物质的性质是解本题的关键,注意基础知识的积累.
本题难度:一般
3、选择题 两种气态烃的混合气体0.1mol,完全燃烧后生成0.16molCO2和3.6g水,则混合气体是
A.一定有丙炔
B.一定是甲烷和乙烯
C.一定没有乙烷
D.一定有乙炔
参考答案:C
本题解析:分析:n(H2O)=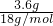 =0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
则混合烃的平均分子式为C1.6H4,根据平均分子式进行判断.
解答:n(H2O)=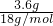 =0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
则混合烃的平均分子式为C1.6H4,烃中C原子数小于1.6的只有甲烷,则一定含有甲烷,CH4分子中含4个氢原子,故另一种分子中一定含4个氢原子,且其碳原子数大于1.6,故可能是C2H4或C3H4,一定没有C2H6或C2H2,二者的H原子不等于4,
故选C.
点评:本题考查混合烃组成的判断,题目难度中等,本题关键是能够正确分析有机物完全燃烧生成的CO2和H2O的物质的量关系,根据平均分子式进行判断.
本题难度:一般
4、选择题 将铁片放入下列溶液中,铁片溶解且固体质量减少,并无气体产生,则该溶液是
A.CuSO4溶液
B.稀HNO3溶液
C.Fe2(SO4)3溶液
D.Al2(SO4)3溶液
参考答案:C
本题解析:A、发生置换反应,质量增加;B、溶解,产生气体NO;C、溶解生成二价铁,正确;D、不反应。
本题难度:困难
5、选择题 下列物质长期露置于空气中会变质但不发生氧化还原反应的是
A.Na
B.NaOH
C.Na2CO3
D.氯水
参考答案:B
本题解析:分析:空气中含有二氧化碳和氧气等,能与二氧化碳或氧气反应的物质能变质,在光照条件下能分解的物质也能变质,在化学变化过程中有元素化合价变化的反应是氧化还原反应,据此结合发生的反应判断;
解答:A.Na与氧气反应生成氧化钠,反应中钠元素、氧元素的化合价发生变化,属于氧化还原反应,故A不符合;
B.在空气中NaOH潮解,与二氧化碳反应生成碳酸钠,没有发生氧化还原反应,故B符合;
C.Na2CO3在空气中不变质,故C不符合;
D.氯水中含有HClO,不稳定,见光分解生成HCl和O2,发生氧化还原反应,故D不符合;
故选:B.
点评:本题考查物质的性质以及氧化还原反应,题目难度不大,注意把握常见物质的性质以及氧化还原反应的判断方法.
本题难度:困难