微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 现有四种元素基态原子的电子排布式为:①1s22s22p63s1 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5,则下列有关比较中正确的是 [???? ]
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>②>③>①
D.最高正化合价:④>③=②>①
参考答案:A
本题解析:
本题难度:一般
2、选择题 下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
选项
| 陈述Ⅰ
| 陈述Ⅱ
| 判断
|
A
| 盛放氢氧化钠溶液的试剂瓶用橡胶塞
| 氢氧化钠可以与玻璃中的二氧化硅反应生成粘性的硅酸钠
| Ⅰ对,Ⅱ错,无
|
B
| 氯水可以使有色布条褪色
| 氯气具有漂白性
| Ⅰ错,Ⅱ对,有
|
C
| 二氧化硅可以与水反应生成硅酸
| 二氧化硅是酸性氧化物具有酸性氧化物的通性
| Ⅰ对,Ⅱ对,无
|
D
| 为增强漂白能力使用漂白粉时向漂白粉溶液中加入少量白醋
| 醋酸的酸性比次氯酸强
| Ⅰ对,Ⅱ对,有
参考答案:D
本题解析:
试题分析:A:氢氧化钠可以与玻璃中的二氧化硅反应生成粘性的硅酸钠所以要用橡胶塞,表述I、II都正确;B:氯水使有色布条褪色是因为生成次氯酸,不是氯气具有漂白性;C:酸性氧化物对应的水化物是酸,二者有联系;D:漂白粉的主要成分是次氯酸钙,漂白原理是次氯酸钙与酸反应产生的次氯酸生效,根据强酸制弱酸的原理,加入白醋能增强漂白能力,D正确。
点评:此题考核了常见化学物质的性质,体现了结构决定性质,性质决定用途的思想,学生要在平常的学习中,学会归纳,此题终合性较强,难度中等。
本题难度:一般
3、选择题 下列各组物质的性质比较,正确的是[???? ]
A.酸性:HClO4>H3PO4>H2SO4
B.氢化物稳定性:HF>H2O >H2S
C.碱性:NaOH>Mg(OH)2>Ca(OH)2
D.原子半径:F>Cl>Br>I
参考答案:B
本题解析:
本题难度:一般
4、选择题 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示[部分产物略去,Fe能与足量稀HNO3反应生成Fe(NO3)3]。下列说法错误的是
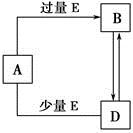
A.A、B、D可能是钠及其化合物
B.A、B、D可能是铁及其化合物
C.A、B、D可能是铝及其化合物
D.A、B、D不可能是非金属及其化合物
参考答案:D
本题解析:选项A,A为NaOH、B为NaHCO3、D为Na2CO3、E为CO2时满足框图转化关系;选项B,A为Fe、E为稀硝酸、D为Fe(NO3)2、B为Fe(NO3)3时满足框图转化关系;选项C,A为AlCl3、E为NaOH、B为NaAlO2、D为Al(OH)3时满足框图转化关系;选项D,A为C、E为O2、B为CO2、D为CO时满足框图转化关系,所以A、B、D可能是非金属及其化合物。
本题难度:一般
5、选择题 下列各组元素属于p区的是
A.Na、N、P
B.O、S、Ar
C.Fe、Ar、Cl
D.H、Mg、Al
参考答案:B
本题解析:
本题难度:一般
|