ϡ����
�ο��𰸣�A
�������������ԭ��صĹ��ɡ�����ԭ��ص������ǻ����Բ�ͬ�Ľ���������ͷǽ�������������������������Һ�С�A���Ҵ����ǵ���ʣ����Բ��ܹ���ԭ��ء���ѡA��
�����Ѷȣ���
2��ѡ���� һ����������ȼ�ϵ�ؿ�������ˮ��������ˮ�������乤��ԭ����ͼ��ʾ������˵������ȷ����
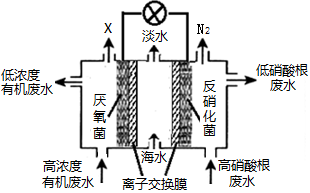
A�����Cl����������
B��X����ΪCO2
C��������ĺ��������ˮpH����
D����·��ÿͨ��1 mol���ӣ�������״���µ��������Ϊ2.24L
�ο��𰸣�C
���������
���������A���Ҳ�缫����������˵��NԪ�صĻ��ϼ۴�+5�۽��͵�0�ۣ�������ԭ��Ӧ��������ԭ��ص������������Ϊ�������������������ƶ����м���Cl���������ң���ȷ��B�����Ϊ����������������Ӧ�����л���ˮ�е�CԪ�صĻ��ϼ����ߣ�����������������ת��Ϊ������̼���壬��ȷ��C�����������ķ�Ӧ��2NO3-+12H++10e-=N2+6H2O�����Դ�����ķ�ˮ������Ũ�ȼ�С����pH���ߣ�����D��������������ӷ�Ӧ�ĵ缫��Ӧʽ��ÿͨ��1mol���ӣ�������0.1mol��������״���µ������2.24L����ȷ����ѡC��
���㣺����绯ѧ��Ӧ��Ӧ��
�����Ѷȣ�һ��
3��ѡ���� Ŀǰ���������˿ɳ��п��������ؼ���,ʹ���ֵ�����˸��㷺����;�����ֵ��ʹ�����⼼�����������е���,�Կ�����Ϊ�����,��طŵ�ʱ���ܷ�ӦΪ2Zn+O2 2ZnO,�����ж���ȷ����(����) 2ZnO,�����ж���ȷ����(����)
A���ŵ�ʱ,OH-�������ƶ�
B���ŵ�ʱ,������ӦʽΪZn+2OH--2e- ZnO+H2O ZnO+H2O
C�����ʱ,Zn����������Ӧ
D�����ʱ,������ӦΪO2+2H2O+4e- 4OH- 4OH-
�ο��𰸣�A
���������ԭ��طŵ�ʱ����������,��������������,A����ȷ;��ԭ�����ZnΪ����,��������ӦʽΪO2+4e-+2H2O 4OH-,B�����;���ʱ,ZnO������ԭ��Ӧ,OH-����������Ӧ,C�����;���ʱ������ӦʽӦΪZnO+H2O+2e- 4OH-,B�����;���ʱ,ZnO������ԭ��Ӧ,OH-����������Ӧ,C�����;���ʱ������ӦʽӦΪZnO+H2O+2e- �����Ѷȣ�һ�� �����Ѷȣ�һ��
4������� ��6�֣�������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ�����Li2CO3��Na2CO3�͵������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650���¹�����ȼ�ϵ�أ�����йصĵ�ط�Ӧʽ����ط�Ӧʽ��������Ӧʽ��2CO+2CO32- ��4CO2+4e-��
������Ӧʽ��????????????????????��
����ܷ�Ӧ��????????????????????????????��
�ο��𰸣�
 ��������� ���������
��д���ܷ�Ӧ��2CO��O2=2CO2,��ȥ������Ӧ����������Ӧʽ��O2��2CO2��4e�D=2CO32�D
�����Ѷȣ�һ��
5��ѡ���� ������ƽ�����Pt˿���缫����KOH��Һ�У�Ȼ���������Ϸֱ�ͨ�����������������ȼ�յ�ء��õ���з�Ӧ�Ļ�ѧ����ʽΪ��CH4+2O2+2KOH==K2CO3+3H2O������ڴ�ȼ�ϵ�ص�����˵��������ǣ�����������������Ϊ1��6��10-19C��[???? ]
A��ͨ������ĵ缫Ϊ��صĸ�����ͨ�������ĵ缫Ϊ����
B���ڱ�״���£�ÿ����5��6LO2���������ṩԼ9��6��104C�ĵ���
C��ͨ������缫�ĵ缫��ӦΪ��CH4+10OH-��8e-====CO32- +7H2O
D���ŵ�һ��ʱ�����Һ��pHֵ����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
|