��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1���֣�
һλͬѧ�ڸ�ϰʱ��������һ��ϰ�⣺ij��ɫ��Һ�п��ܺ��С�H+��OH-��Na+��NO3-�����������ۺ�ֻ����H2���ʸ���ɫ��Һ���ܴ��������ļ������ӡ�
��1���������۲���H2��˵��������______��������ԡ���ԭ�ԡ�����
��2����ͬѧ��������H+�������ڣ���NO3-�Ͳ��ܴ������ڡ�
���ʵ��֤ʵ���£�
װ ��
| �� ��
|
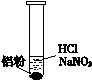
| ��. ʵ���ʼ��δ����������
��. ��һ������������ݣ�Һ���Ϸ���dz��ɫ
��. �Թܱ��ȣ���Һ����
???
�� �����ܽ�Al2O3��Ĥ�����ӷ���ʽ��______��
�� ���������Ʋ���Һ�в�����NO��Ϊ��һ��ȷ�ϣ���������ʵ�飺
ʵ?��
| ��?��
| ��?��
| ʵ��1
| ?��ʪ��KI��������ֽ���ڿ�����
| ���
| ʵ��2
| ��ʪ��KI��������ֽ����dz��ɫ����
| ��ֽ����
?a. dz��ɫ������______��
b. ʵ��1��Ŀ����_______��
c. ʵ��1��2˵����Ӧ������NO��������NO�����ӷ���ʽ����������
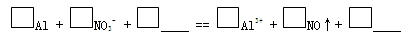
��3���ټ��裺��OH-�������ڣ�NO3-Ҳ���ܲ��ܴ������ڡ�
�������ʵ��֤ʵ���£�
װ ��
| �� ��
| 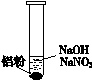
| ��. ʵ���ʼ��δ����������
��. ��һ������������ݣ��д̼�����ζ
?
Ϊȷ�ϡ��̼�����ζ�����壬��������ʵ�飺��ʪ��KI��������ֽ���飬δ��������ʪ���ɫʯ����ֽ���飬��ֽ������
�� �̼�����ζ��������______��
�� ��������������ӷ���ʽ��______��
��4����NaOH��Һ�м������ۣ����ֻ�������H2���ɣ��仯ѧ����ʽ��______��
��5��ʵ����֤ʵ��NO3?���ᡢ���Ի����ж���һ���������ԣ������������ʣ��������������ϰ���е���ɫ��Һһ���ܴ������ڵ���Na+��OH-��
2������� ��10�֣�
��1������һ����Ҫ�Ľ������ϣ����ȷ�Ӧ���Ժ��Ӹֹ죬��д�����ڸ�������������������Ӧ�Ļ�ѧ����ʽ???????????????????????
��2��ij���Ͻ��к��кϽ�Ԫ��þ��ͭ���裬Ϊ�˲ⶨ�Ͻ������ĺ��������������ʵ�飬��ش��й����⣺
�ٳ�ȡ��Ʒag������Ʒ����������ϡ���ᣬ���ˣ�
����Һ�м������������������Һ�����ˣ��йص����ӷ���ʽΪ��?????????????????
�۲���ڵ���Һ��ͨ��������CO2���壬�ɲ���Al��OH��3����
�ܲ���۹��˺������������ˮϴ�����Σ���ɲ����������أ���ȴ�������������Ϊbg��ԭ��Ʒ��������������Ϊ???????????
��3����ҵ�ϣ������ڵ�¯����̿�ۻ�ԭ������̼���Ƶõģ�д���÷�Ӧ�Ļ�ѧ����ʽ
????????????????????????????????????��������¯�м���12g�������������̿�۵Ļ������ɵ������ڱ�״���µ����Ϊ????????????????��
3��ѡ���� �����й����ʵ����ʺ����ʵ�Ӧ�þ���ȷ���ǣ�������
A���������а뵼�����ʣ��������������ά
B������������Ư���ԣ������ڼӹ�ʳƷʹʳƷ����
C��ͭ�Ľ�����Ա�����������ͭ������������Ũ����
D�����������õ����ԣ��ֿ���ǿ�ȴ�о�����߿�����Զ�����ѹ����߲���
4��ѡ���� �����йؽṹ�����ʵ�˵���У���ȷ���ǣ�������
A���������ڳ����²�����������Ӧ����������Ʒ����һ���Ŀ���ʴ���ܣ���һ��Ӧ�ù㷺�Ľ�������
B��סFeCl3��Һ�е���KIһ������Һ����Һ����ɫ
C��Ԫ�طǽ�����Cl��S��ʵ������������HCl��H2S
D��ͬ��������Ԫ�ص�ԭ���γɵļ����ӵĵ��Ӳ�ṹһ����ͬ
5������� ij����С���һЩ�������ʺͻ���������ʽ����о���
��1���±�Ϊ�������Ȼ�ͭ��Һ��Ӧ��ʵ�鱨���һ���֣�
ʵ�鲽��
| ʵ������
| �ٽ���ĥ������Ƭ������������һ��Ũ�ȵ�CuCl?2��Һ�С�
| �������ݣ��������ɵĺ�ɫ���壬��Һ��Ϊ��ɫ��
| �ڷ�Ӧ������������Һ���á�
| ?
| �ۺ�ɫ����������ˮϴ�Ӻ����ڳ�ʪ�����С�
| һ��ʱ�������ɺ�ɫ��Ϊ��ɫ[������Ҫ�ɷ�ΪCu2(OH)2CO3]��
?
��ʵ���з�����Ӧ������д�����л�ѧ����ʽ�������ӷ�Ӧ��ֻд���ӷ���ʽ��
���������ɵĺ�ɫ����????????????????????????????????????????????????��
��һ��ʱ�������ɺ�ɫ��Ϊ��ɫ??????????????????????????????????????��
��2����ʯī���缫���������ʵ����������Һ�������������ݡ�������⣬��������������Һ�л��ɹ۲쵽��������????????????????????????????????????????????????????????????????????????????��
���ʹ���������ӷ���ʽ��???????????????????????????��????????????????????????????????��
��3����ҵ�Ͽ����������̿���Ҫ�ɷ�ΪMnO2����Ӧ�����������̡�
�����������̿�ұ���̵�ԭ���ǣ��û�ѧ����ʽ��ʾ��
???????????????????????????????????????????????????????????????????��
��MnO2��H2O2�ֽⷴӦ������������������MnO2�����ữ���H2O2��Һ�У�MnO2�ܽ����Mn2+���÷�Ӧ�����ӷ���ʽ��???????????????????????????????????????????????????????????????????��
|
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772
|