微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某同学用中和滴定法测定某烧碱样品的纯度,其操作步骤如下:
①称取25.0g烧碱样品,配成1L溶液;
②用????????????????(填仪器名称)量取10. 00mL配制好的溶液于锥形瓶中,用0.20mol・L-1的标准盐酸滴定(杂质不与盐酸反应),所得数据如下表,其中第2组数据读数如图所示。
滴定序 号
| 待测液体积/mL
| 所消耗盐酸标准液的体积/mL
|
滴定前
| 滴定后
| 消耗的体积
|
1
| V
| 0.50
| 25.52
| 25.02
|
2
| V
| ??????????
| ??????
| ????????
|
3
| V
| 1.00
| 25.98
| 24.98
?????????????????????????????????????????????????????????
请回答下列问题:
(1)根据滴定管的读数填写上表。
(2)实验过程中,配制溶液定容时俯视刻度线会使所配溶液浓度?????????(填“偏大”“偏小”或“无影响”,下同);滴定前仰视液面,滴定后平视液面会使烧碱样品纯度的测量值比实际值??????????。
(3)三组数据中,因误差过大而应舍去的一组是第???????组(填序号),根据合理数据求得该烧碱样品中NaOH的质量分数为????????????。
2、简答题 侯德榜先生是我国举世闻名的化工专家,他对制碱技术作出了重大贡献,他所发明的联合制碱法称作“侯氏制碱法”.右图是在实验室中模拟“侯氏制碱法”中制取碳酸氢钠一步的实验装置,实验步骤为:
①连接好装置,检验气密性,在仪器内装入药品.
②先从D的分液漏斗中连续滴下浓氨水,直到产生的气体不能再在C中的饱和NaCl溶液中溶解时.再通入A中产生的气体.片刻后,烧杯中析出白色固体(碳酸氢钠).继续向C中通入两种气体,直到不再有固体产生为止.
③过滤烧杯内所得的混合物,得到碳酸氢钠固体.
④向滤液中加入适量的氯化钠固体,发生反应:
NaCl(s)+NH4Cl(aq)=NaCl(aq)+NH4Cl(s),搅拌后过滤,滤出物可用作化肥.
⑤滤液再注入烧杯C中,重复使用,进行下一次制备…
试回答下列问题:
(1)检验装置A气密性的方法是______.
(2)烧杯C中发生反应的化学方程式为______.
(3)A中常选用的固体为______;B中应选用的液体为______.
(4)步骤②中必须先让D中发生反应,产生气体后,再让A中发生反应产生气体,原因是______.
(5)步骤④是在较高温度(如60℃)下还是在较低温度下(如0℃~10℃)下进行合适?______(填“较高”或“较低”)
(6)步骤④中所得的氯化铵晶体中常含有少量的氯化钠和碳酸氢钠(约占5%~8%),请设计简单的实验证明所得固体的成分大部分是氯化铵.简要写出操作方法、现象和结论.______.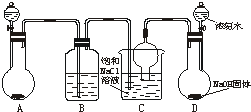
3、选择题 下列实验操作中,错误的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。
B.蒸馏时,应使温度计水银球位于蒸馏烧瓶支管处。
C.用酒精萃取碘水溶液中的碘。
D.过滤时漏斗下端应与烧杯内壁紧靠。
4、选择题 下列有关实验操作或判断正确的有
①用10 mL量筒准确量取稀硫酸溶液8.0 mL;
②用干燥的pH试纸测定氯水的pH;
③能说明亚硝酸是弱电解质的是:用HNO2溶液作导电试验,灯泡很暗
④使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大;
⑤将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体;
⑥圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
⑦除去铁粉中混有的少量铝粉.可加人过量的氢氧化钠溶液,完全反应后过滤
⑧为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
⑨用食醋除去水壶中的水垢
A.3个
B.4 个
C.5个
D.6个
5、选择题 下列有关说法正确的是(???? )
①进行中和热的测定实验时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度②用滴定管量取盐酸前,先用蒸馏水洗净后再用待取盐酸进行润洗③用蒸馏装置可以制乙酸乙酯,但温度计的水银球应放入液体中④蔗糖水解实验,用NaOH中和稀硫酸之后再用新制的氢氧化铜检验是否水解
A.②③
B.①③
C.①②④
D.①②
|