微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法错误的是( )
A.元素的电子层数越多,其原子半径一定越大
B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C.除氦外的稀有气体原子的最外层电子数都是8
D.铊(Tl)与铝同主族,其单质肯定能与盐酸反应
参考答案:A、元素的电子层数越多,其原子半径不一定越大,如锂原子半径>
本题解析:
本题难度:简单
2、填空题 “空气质量日报”中空气污染指数的项目包含:SO2、CO、NO2、O3和可吸入颗粒物等。
(1)血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
①写出亚铁离子的基态电子排布式???????????。
②根据等电子体原理,1个CO分子中含有的π键数目为????????????。
(2)为减轻SO2污染,火力发电厂生产中常在燃煤中加入CaO以“固硫”。科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其晶格能数据如下表:
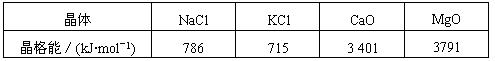
①4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是??????????????。
②4种晶体的配位数均为???????????????。
(3)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注。
甲醛(HCHO)是室内主要空气污染物之一(其沸点是-19.5℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高于甲醛的主要原因
是:????????????????。甲醛分子中碳原子的杂化方式是??????????。
参考答案:
(1)①[Ar]3d6??? ②2
(2)①M
本题解析:略
本题难度:简单
3、选择题 在下列分子结构中,有原子的最外层电子不能满足8电子稳定结构的是 [???? ]
A.N2?????? ????
B.PCl3?????? ? ?
C.BF3????? ?
D.CO2
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列叙述正确的是[???? ]
A.含有离子键的化合物一定是离子化合物
B.含有共价键的化合物一定是共价化合物
C.离子化合物中不可能含有共价键
D.共价化合物中可能含有离子键
参考答案:A
本题解析:
本题难度:简单
5、选择题 氢键既可以存在于分子之间,也可以存在于分子内部的原子团之间,如邻羟基苯甲醛分子( ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( HO
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( HO CHO )之间存在氢键(分子间氢键)。则两者的熔点、沸点的相对大小关系是(????)
CHO )之间存在氢键(分子间氢键)。则两者的熔点、沸点的相对大小关系是(????)
A.前者>后者
B.前者<后者
C.前者=后者
D.无法估计
参考答案:B
本题解析:
试题分析:由于分子间氢键强于分子内的氢键,所以邻羟基苯甲醛的熔沸点小于对羟基苯甲醛熔沸点,答案选B。
点评:该题是常识性知识的考查,试题基础性强,紧扣教材基础知识,意在调动学生的学习兴趣和学习积极性,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般