微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是 和 (填分子式)。
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为 0.021 6 mol/L。
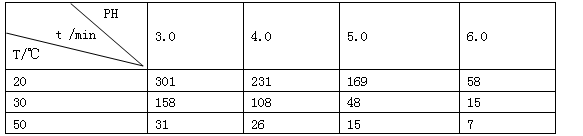
①pH增大能加速O3分解,表明对O3分解起催化作用的是 。
②在30℃、pH=4.0条件下,O3的分解速率为 。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为 (填字母代号)。
A.40 ℃、pH=3.0 B.10 ℃、pH=4.0 C.30 ℃、pH=7.0
参考答案:(1)O2、I2;
(2)①OH-;②1.00×10-
本题解析:
试题分析:(1)O3与KI溶液反应不可能生成K单质,故生成的两种单质只能为O2、I2。
(2)①由表中数据可知:pH由3.0到6.0增大,O3分解速率加快,则OH-浓度增大,化学反应速率加快,所以表明OH-对O3分解起催化作用;
②在30℃、pH=4.0条件下,O3的分解速率为:v=△c/△t=0.0108mol/L=1.00×10-4mol/(L・min);
③由表中数据可知,40°C、pH=3.0时,所需时间t1:31min<t1<158min之间;10°C、pH=4.0时,所需时间t2>231min;30°C、pH=7.0时,所需时间t3<15min,则分解速率依次增大的顺序为b<a<c;
考点:了解化学反应速率的概念、反应速率的定量表示方法。理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识并能用相关理论解释其一般规律。
点评:考查影响速率的因素,培养学生分析利用实验数据的能力。
本题难度:一般
2、填空题 反应A(g)+B(g)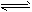 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
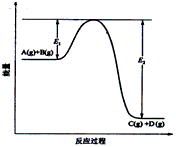
(1)该反应是_____________反应(填“吸热”“放热”)
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),原因是________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?________,原因是_________________________
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
参考答案:(1)放热
(2)减小;该反应正反应为放热反应,升高温
本题解析:
本题难度:一般
3、填空题 下表是稀硫酸与某金属反应的实验数据:
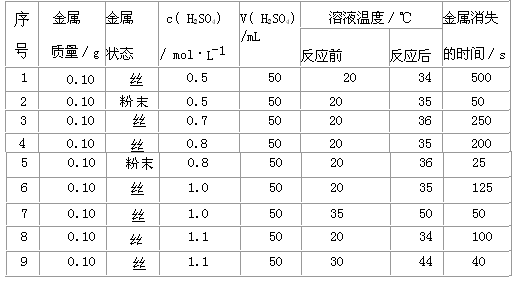
分析上述数据,回答下列问题:
(1)实验4和5表明,___________对反应速率有影响,________反应速率越快,能表明同一规律的实验还有________________________________ (填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有_____________(填实验序号);
(3)本实验中影响反应速率的其他因素还有____________,其实验序号是___________
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:_____________________________________________________ 。
参考答案:(1)固体反应物的表面积;表面积越大;l和2?
(2)
本题解析:
本题难度:一般
4、填空题 在容积可变的密闭容器中,可逆反应2HI(g) H2(g)+I2(g)已达平衡,若将体积缩小,在缩小的过程中:
H2(g)+I2(g)已达平衡,若将体积缩小,在缩小的过程中:
(1)正反应速率______________;
(2)逆反应速率______________;
(3)平衡______________;
(4)容器内颜色______________;
(5)H2的质量分数______________;
(6)混合气体的平均相对分子质量______________;
(7)H2的浓度______________;
(8)HI的分解率______________;
(9)混合气体的密度______________;
(10)混合气体的质量______________。(用“变大”“变小”“不变”“加深”“变浅”填写)
参考答案:
 本题解析:略
本题解析:略
本题难度:简单
5、实验题 将Zn投入一定浓度一定体积的盐酸中,H2的生成速率与时间的关系如图所示,试解释图中曲线变化的原因(纵坐标为H2的生成速率,横坐标为时间)。
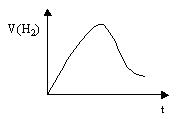
答:① ;
② 。
参考答案:①反应开始时,反应放热,反应速率较快;②随着反应的进行,HC
本题解析:本题能力层次为C。Zn与盐酸反应是放热反应,该反应中影响化学反应速率的因素有两个:一是反应放出的热量使反应速率增大;二是反应使HCl物质的量浓度减小,反应速率减小。由图像可知,在开始时温度变化是影响反应速率的主要因素,但随着反应的进行,HCl物质的量浓度的减小是影响反应速率的主要因素。答案:①反应开始时,反应放热,反应速率较快;②随着反应的进行,HCl物质的量浓度变小,反应速率又变慢.
学法指导:本题考查通过图像分析影响化学反应速率的因素。图像分析应注意以下几方面:(1)看起点(2)看终点(3)看变化趋势,分清“渐变”和“突变”,“大变”和“小变”等。
本题难度:简单