微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对可逆反应N2(g)+3H2(g) 2NH3(g),△H=-92.4 kJ.mol-1下列叙
2NH3(g),△H=-92.4 kJ.mol-1下列叙
述正确的是
A.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
B.若单位时间内消耗x mol N2,同时生成2x mol NH3,则反应达到平衡状态
C.若达到平衡时,共放出46.2kJ热量,则有l mo1NH3(g)生成
D.达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍
参考答案:C
本题解析:升高温度,正逆反应速率都增大,A错;B中只是说明了平衡正向逆方向进行,
无法判断正反应速率与逆反应速率是否相等,B错;放出的热量是92.4的一半,
则生成NH3为1mol,C正确;容器体积缩小为原来的一半,则平衡向正向移动,
则c(NH3)大于原来的2倍,D错;答案选C。
本题难度:一般
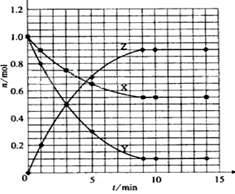
2、选择题 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是(???)
A.反应的化学方程式是X+2Y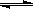 2Z
2Z
B.该反应在0-3min时间内产物Z的平均反应速率0.083mol・L-1・min-1
C.在3分钟时Y和Z的浓度相等
D.其他条件不变,升高温度,若正反应速
率增大,则逆反应速率将减小
参考答案:D
本题解析:由图像可知X、Y的物质的量减少,Z的物质的量增加,所以X、Y是反应物,Z是生成物。反应进行到3min时,X、Y、Z的物质的量分别为0.75mol、0.5mol、0.5mol,即X、Y、Z的变化量分别为0.25mol、0.5mol、0.5mol,所以方程式为X+2Y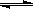 ? 2Z。反应在0-3min时间内产物Z的平均反
? 2Z。反应在0-3min时间内产物Z的平均反
本题难度:一般
3、实验题 已知氯水中有如下平衡:Cl2+H2O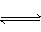 HCl+HClO。常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O。
HCl+HClO。常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O。
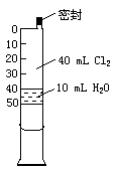
(1)针筒中可观察到的现象是________________。
(2)若将此针筒长时间放置在有日光的地方,最终可能观察到的现象是________________。
(3)用化学平衡的观点解释(2)的现象:________________。
参考答案:(1)气体体积缩小,溶液呈浅黄绿色;
(2)气体和
本题解析:正确分析出该装置中所发生的物理化学变化,然后运用外界条件对化学平衡移动的影响来解释。其中主要化学变化为:Cl2+H2O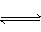 HCl+HClO,2HClO
HCl+HClO,2HClO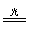 本题难度:一般
本题难度:一般
4、选择题 对于反应2 SO2 + O2 2SO3 ,下列变化可以增大活化分子百分率使反应速率加快的是
2SO3 ,下列变化可以增大活化分子百分率使反应速率加快的是
① 加压??????② 升温????③ 充入N2??????④ 使用催化剂
A.①②
B.②③
C.②④
D.①②③④
参考答案:C
本题解析:略
本题难度:简单
5、填空题 (15分)碳及其化合物有广泛的用途。
(1)在电化学中,常用碳作电极。在碱性锌锰干电池中,碳棒作????极。
(2)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)=CO(g)+H2(g);△H=+131.3kJ?mol-1,则要制备标准状况下22.4升水煤气,转移的电子的物质的量为???,需要吸收的热量为?????????kJ。
(3)工业上把水煤气中的混合气体经过处理后,获得的较纯H2用于合成氨:
N2(g)+3H2(g) 2NH3(g);△H=-92.4kJ?mol-1。下图1是在两种不同实验条件下模拟化工生产进行实验所测得N2随时间变化示意图。
2NH3(g);△H=-92.4kJ?mol-1。下图1是在两种不同实验条件下模拟化工生产进行实验所测得N2随时间变化示意图。
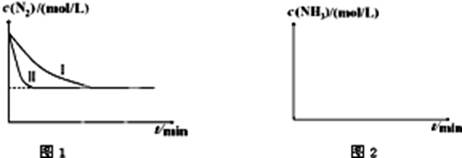
①与实验Ⅰ比较,实验Ⅱ改变的条件为:????????????????????????。
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在上图2中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图。
(4)Na2CO3可在降低温室气体排放中用作CO2的捕捉剂。1L0.2mol/L Na2CO3溶液吸收标准状况下2.24LCO2后,溶液中各离子浓度由大到小的顺序为???????????。
参考答案:(1)正;???(2)1mol ;65.65KJ?;
本题解析:
试题分析:(1)在电化学中,常用碳作电极。在碱性锌锰干电池中,碳棒作正极,Zn皮作负极。(2)根据反应方程式可知:每产生2mol的水煤气,转移电子2mol。现在要制备标准状况下22.4升水煤气,即制取1mol气体,所以转移的电子的物质的量为1mol;需要吸收的热量为131.3KJ÷2=65.65KJ;(3)①与实验Ⅰ比较,实验Ⅱ达到平衡所需要的时间缩短,但是平衡时物质的浓度没变,因此改变的条件为:使用催化剂。②若其它条件相同,实验Ⅲ比实验Ⅰ的温度要高,由于升高温度,化学反应速率加快,所以达到平衡所
本题难度:一般