微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是

A.图中a点对应的是AgBr的不饱和溶液
B.在t℃时, Ksp(AgBr) =4.9×10-13
C.在t℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
D.在AgBr的饱和溶液中加入NaBr固体,可使溶液由b点到c点
参考答案:D
本题解析:
试题分析:根据图示可知:在线上的点,为饱和溶液,在线作下方的点溶液未达到饱和,在线右上方的点是过饱和溶液。A.图中a点在线的左下方,由于c(Br-)・c(Ag+)<Ksp(AgBr)=4.9×10-13,所以对应的是AgBr的不饱和溶液,正确;B.在t℃时, Ksp(AgBr) = c(Br-)・c(Ag+)=4.9×10-13,正确;C. t℃时AgCl的Ksp=4×10-10,c(Cl-)= c(Ag+)=2×10-5,Ksp(AgBr) = c(Br-)・c(Ag+)=4.9×10-13,则AgCl(s)+ Br-(aq)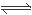 AgBr(s)+Cl-(aq)的平衡常数K= c(Cl-)÷c(Br-)=Ksp(AgCl)÷Ksp(AgBr)= 4×10-10÷4.9×10-13≈816,正确;D.在AgBr的饱和溶液中加入NaBr固体,沉淀溶解平衡仍然存在,由于c(Br-)增大,所以平衡逆向移动,c(Ag+)减小,但是二者的乘积不变,只能是线上的点,溶液不可能由b点到c点,错误。
AgBr(s)+Cl-(aq)的平衡常数K= c(Cl-)÷c(Br-)=Ksp(AgCl)÷Ksp(AgBr)= 4×10-10÷4.9×10-13≈816,正确;D.在AgBr的饱和溶液中加入NaBr固体,沉淀溶解平衡仍然存在,由于c(Br-)增大,所以平衡逆向移动,c(Ag+)减小,但是二者的乘积不变,只能是线上的点,溶液不可能由b点到c点,错误。
考点:考查图像法在表示沉淀溶解平衡及溶液中离子浓度、溶液的饱和程度的应用的知识。
本题难度:一般
2、选择题 下列有关Ksp的叙述中正确的是(?)
A.Ksp越大说明电解质的溶解度越大
B.Ksp只与电解质的本性有关,而与外界条件无关
C.Ksp表示难溶强电解质在水中达到沉淀溶解平衡时,溶液中离子浓度幂之积
D.Ksp的数值只与难溶电解质的性质有关,和温度无关
参考答案:C
本题解析:溶度积常数大,但溶解度不一定大,选项A不正确;Ksp除与电解质的本性有关,还与温度有关系,选项B和D都是不正确的,因此正确的答案选C。
本题难度:一般
3、填空题 (10分)金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,?控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(s,mol・L-1)见图。
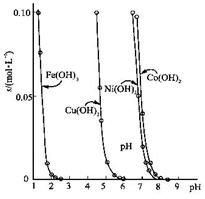
(1)pH=3时溶液中铜元素的主要存在形式是:??????????????(写化学式)
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为??????????(填字母)
A、<1???? B、4左右???? C、>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,????(能、不能)通过调节溶液pH的方法来除去,理由是????????????
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以 加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式。?????????????????????????????????
加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式。?????????????????????????????????
(5)已知一些难溶物的溶度积常数如下表。
物质
| FeS
| MnS
| CuS
| PbS
| HgS
| ZnS
|
Ksp
| 6.3×10-18
| 2.5×10-13
| 1.3×10-36
| 3.4×10-28
| 6.4×10-53
| 1.6×10-24
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的????除去它们的是??????。(选填序号)
A、NaOH???? B、FeS???? C、Na2S
参考答案:(9分)
 本题解析:略 本题解析:略
本题难度:一般
4、填空题 试利用平衡移动原理解释下列事实:
(1)FeS不溶于水,但能溶于稀盐酸中;
(2)CaCO3难溶于稀硫酸,却能溶于醋酸中;
(3)分别用等体积的蒸馏水和0.010 mol・L-1硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量。
参考答案:(1)FeS(s) 本题解析:详见答案 本题解析:详见答案
本题难度:一般
5、选择题 Mg(OH)2在下列四种情况下,其溶解度最大的是(??? )
A.在纯水中
B.在0.1 mol・L-1的MgCl2溶液中
C.在0.1 mol・L-1的NH3・H2O中
D.在0.1 mol・L-1的CH3COOH溶液中
参考答案:D
本题解析:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),加入MgCl2和NH3・H2O均能抑制Mg(OH)2的溶解,加入CH3COOH能促进Mg(OH)2溶解,故选D。 Mg2+(aq)+2OH-(aq),加入MgCl2和NH3・H2O均能抑制Mg(OH)2的溶解,加入CH3COOH能促进Mg(OH)2溶解,故选D。
本题难度:简单
|