微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 t℃时,在两个相同的密闭刚性容器(等容)中分别进行SO2和SO3相互转化的实验,反应的化学方程式为2SO2(g)+O2(g) 2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所示:
2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所示:
数据分析发现:达到平衡时,化学状态Ⅰ和化学状态Ⅱ完全相同。下列叙述不正确的是
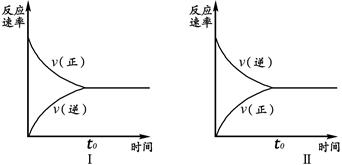
A.若实验ⅠSO?2的起始浓度为1mol/L,则实验ⅠO2的起始浓度为0.5mol/L;实验ⅡSO3的起始浓度为1mol/L.
B.若实验ⅠSO2的转化率为a%,则实验ⅡSO3 的转化率为1-a%。
C.若起始浓度C(SO2) m mol/L,C(O2)=" n" mol/L,C(SO3)=" p" mol/L,在相同条件下进行实验,要求达到平衡时的状态与实验Ⅰ、Ⅱ完全相同,则m、n、p必须满足的条件是m/n="2" 和 m+p=1。
D.维持实验Ⅰ的起始浓度和实验温度不变,改密闭刚性容器为密闭可变体积容器(等压容器)进行实验,达到化学平衡时:SO2的转化率与实验Ⅰ中SO2的转化率相比要小,但正反应速率与实验Ⅱ相比要大。
参考答案:D
本题解析:
试题分析:从实验Ⅰ中起初V(逆)为0,说明只有反应物,没有生成物,而实验Ⅱ中起初V(正)为0,说明只有生成应物,没有反应物.数据分析发现:达到平衡时,化学状态和化学状态二完全相同,也就是等温和等容条件下的等效平衡。由于图Ⅱ中隐含一个条件,只有产物,达到平衡时,C(SO2): C(O2)=2:1。SO2的起始浓度为1mol/L,则实验ⅠO2的起始浓度为0.5mol/L,在定T、V条件下,只要通过可逆反应的化学计量数比换算成平衡时左右两边同一边物质的物质的量与原平衡相同,则二平衡等效,即实验ⅡSO3的起始浓度为1mol/L。恒温恒容下分别进行下列两种操作SO2的转化率+SO3的转化率=1,实验ⅡSO3的转化率为1-a%;若起始浓度C(SO2)=" m" mol/L,C(O2)=" n" mol/L,C(SO3)=" p" mol/L,,在相同条件下进行实验,要求达到平衡时的状态与实验Ⅰ、Ⅱ完全相同即m/n =" 2" 和 m+p="1;" 改密闭刚性容器为密闭可变体积容器(等压容器)相当于在原来平衡的基础上加压,则加压平衡向正反应方向移动,速率(正逆)变大
点评:本题在掌握化学平衡的相关知识的同时,还应该注意看懂图像,作答时,应该注重图像与知识的结合。难度较大。
本题难度:简单
2、简答题 把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),经5min达到平衡,此时生成2molC,测得D的平均反应速率为0.15mol?(L?min)-1,则平衡时A的物质的量浓度是______;B的转化率是______;x的值是______;平衡混合物中B的体积分数是______(保留一位小数).
参考答案:(1)△n(A)=
本题解析:
本题难度:一般
3、选择题 在容积一定的密闭容器中,反应A(g)+2B(g) 2C(g)达平衡,设初始A、B的物质的量分别为Xmol、Ymol,若要使平衡时反应物总物质的量与生成物总物质的量相等,则X/Y应满足的是
2C(g)达平衡,设初始A、B的物质的量分别为Xmol、Ymol,若要使平衡时反应物总物质的量与生成物总物质的量相等,则X/Y应满足的是
A.1 <X/Y<3????????????????????????? B.3< X/Y <4
C.0.25< X/Y <1.5???????????????????D.0.25< X/Y <0.5
参考答案:C
本题解析:
试题分析:令参加反应的X的物质的量为n,
X(g)+2Y(g) 2Z(g),
2Z(g),
开始(mol):x ??????y ??????????????0
转化(mol):n ?????2n?????????????2n
平衡(mol):x-n???y-2n???????????? 2n
平衡时反应物总物质的量与生成物总物质的量相等,所以有x-n+y-2n=2n,解得n=(X+Y)/5;
反应物不能完全反应,所以有x>n,y>2n,即x>(X+Y)/5 (1),y>2(X+Y)/5 (2)
解(1)得:X/Y>1/4
解(2)得:X/Y<3/2
所以1/4<X/Y<3/2。即0.25< X/Y <1.5。
故选C。
点评:本题考查的是化学平衡的综合应用能力极值法的应用。难度稍难。关键在于利用反应物不能完全反应,列不等式。
本题难度:一般
4、填空题 将1molI2(g)和2molH2置于5L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) 2HI(g) ΔH<0,并达到平衡。HI的体积分数w(HI)随时间变化如曲线(Ⅱ)所示:
2HI(g) ΔH<0,并达到平衡。HI的体积分数w(HI)随时间变化如曲线(Ⅱ)所示:
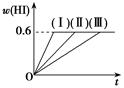
(1)达到平衡时,I2(g)的物质的量浓度为________。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ)所示,在乙条件下w(HI)的变化如曲线(Ⅲ)所示。则甲条件可能是____,乙条件可能是________(填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温恒容条件下,加入适当催化剂
参考答案:(1) 0.02mol/L?(2)③⑤;④
本题解析:(1)根据方程式可知,反应前后体积是不变的,所以根据图像可知,生成HI是3mol×0.6=1.8mol,则消耗单质碘是0.9mol,所以平衡时单质碘的浓度是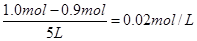 。
。
(2)根据图像可知,曲线I到达平衡的时间最少,说明反应速率快,但平衡是不移动的,所以答案选③⑤;曲线Ⅱ到达平衡的时间最长,说明反应速率慢,但平衡是不移动的,所以答案选④;
本题难度:一般
5、选择题 已知反应:2SO2(g)+O2(g)  ?2
?2 SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
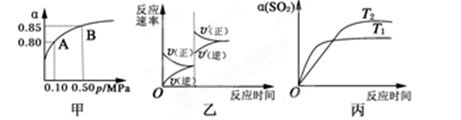
A.由图甲知,A点SO2的平衡浓度为0.4 mol・L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
参考答案:C
本题解析:略
本题难度:一般