微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质在水中能促进水的电离的是(??? )
A.Na2SO3
B.NaOH
C.NaHSO4
D.CH3COONa
参考答案:AD
本题解析:电离出有能水解的离子则对水的电离起促进作用。
本题难度:简单
2、选择题 关于盐类水解的实质,下列叙述正确的是( )
A.盐的电离平衡被破坏
B.水的电离平衡被破坏
C.没有中和反应发生
D.溶液的pH一定变大
参考答案:B
本题解析:盐类水解的实质是盐电离生成的离子与水电离生成的H+或OH-结合生成弱电解质,破坏了水的电离平衡。
本题难度:简单
3、选择题 下列离子方程式正确的是(???)
A.Na2CO3溶液的水解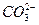 +2H2O
+2H2O H2CO3+2OH-
H2CO3+2OH-
B.金属铝溶于氢氧化钠溶液 Al+2OH-
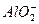 +H2↑
+H2↑
C.铜与浓硝酸反应 3Cu+8H++2
 3Cu2++2NO↑+4H2O
3Cu2++2NO↑+4H2O
D.次氯酸钙溶液中通入过量CO2 ClO-+CO2+H2O====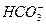 +HClO
+HClO
参考答案:D
本题解析:A中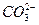 水解应分两步写。B项金属铝溶于氢氧化钠溶液的离子方程式为:2Al+2OH-+2H2O====
水解应分两步写。B项金属铝溶于氢氧化钠溶液的离子方程式为:2Al+2OH-+2H2O==== +3H2↑。C项铜
+3H2↑。C项铜
本题难度:简单
4、选择题 取0.2mol・L-1HX溶液与0.2mol・L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8(25oC),则下列说法(或关系式)正确的是(???)
A.混合溶液中由水电离出的c(OH-)=1×10-8mol・L-1
B.c(Na+)=c(X-)+c(HX)=0.2mol・L-1
C.c(Na+)-c(X-)=9.9×10-7mol・L-1
D.c(OH-)-c(HX)=c(H+)=1×10-6mol・L-1
参考答案:C
本题解析:酸和碱恰好反应,但溶液显碱性,说明HX是弱酸,生成物NaX水解。A不正确,混合溶液中由水电离出的c(OH-)=1×10-6mol・L-1 ;B不正确,应该是c(Na+)=c(X-)+c(HX)=0.1mol・L-1;D不正确,应该是c(OH-)-c(HX)=c(H+)=1×10-8mol・L-1,答案选C。
本题难度:一般
5、选择题 粗制的CuSO4・5H2O晶体中含有Fe2+。提纯时,为了除去Fe2+,常加入少量H2O2, 然后再加入少量碱至溶液pH=4,可以达到除去铁离子而不损失硫酸铜的目的。下列说法不正确的是
A.溶解CuSO4・5H2O晶体时要加入少量稀H2SO4
B.加入H2O2,将Fe2+氧化,2Fe2+ + H2O2 + 2H+ ="=" 2Fe3+ + 2H2O
C.由于CuSO4的催化作用,会使部分H2O2分解而损失
D.调溶液pH=4的依据是Cu(OH)2比Fe(OH)3更难溶
参考答案:D
本题解析:
试题分析:A、溶解CuSO4・5H2O晶体时要加入少量稀H2SO4,防止铜离子水解,正确;B、加入H2O2,将Fe2+氧化,离子方程式正确;C、由于CuSO4的催化作用,会使部分H2O2分解而损失,正确;D、调溶液pH=4的依据是Fe3+沉淀完全时而Cu2+不沉淀,错误,答案选D。4・5H2O晶体中Fe2+的实验分析
本题难度:一般