微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 恒温条件下,在CH3COONa稀溶液中分别加入少量下列物质:①固体NaOH;②固体KOH;③固体
NaHSO4;④固体CH3COONa;⑤冰醋酸。其中一定可使c(CH3COO-)/c(Na+)比值增大的是
[???? ]
A.①②
B.②⑤
C.①⑤
D.②④⑤
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列有关电解质溶液中粒子浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
C.CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-)
D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
参考答案:A
本题解析:
试题分析:A、根据电荷守恒,pH=1的NaHSO4溶液存在:c(Na+)+c(H+)=2c(SO42?)+c(OH?),因为c(Na+)=c(SO42?),所以c(H+)=c(SO42?)+c(OH?),正确;B、含有AgCl和AgI固体的悬浊液:c(Ag+)> c(Cl?)>c(Br?),错误;C、H2CO3的第一步电离大于第二步电离,所以c(H+) > c(HCO3?) >c(CO32?),但c(HCO3?)不等于c(CO32?),错误;D、NaHC2O4和Na2C2O
本题难度:一般
3、填空题 (4分)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏可以降低土壤的碱性。试用化学方程式分别表示盐碱地产生碱性的原因:??????????????????????????????,及用石膏降低其碱性的反应原理:????????????????????????????????????????。
参考答案:(4分) Na2CO3 + H2O= NaOH+NaHCO3
本题解析:
试题分析:碳酸钠是强碱弱酸盐,溶于水水解显碱性,水解方程式是Na2CO3 + H2O= NaOH+NaHCO3;石膏是硫酸钙,能和碳酸钠反应生成难溶性的碳酸钙沉淀,从而抑制水解,反应的化学方程式是Na2CO3 +CaSO4= Na2SO4+CaCO3↓。
点评:本题关键是要从平衡的角度去理解如何降低溶液的酸碱性,因此要利用勒夏特例原理。
本题难度:简单
4、填空题 (1)AgNO3的水溶液呈__________(填“酸”、“中”、“碱”)性, 原因是(用离子方程式表示):___________________;
(2)氯化铝水溶液呈__________性 ,(填“酸”、“中”、“碱”)性, 原因是(用离子方程式表示):________________________。 把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_________。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的_________________。
参考答案:(1)酸;Ag++H2O![]() 本题解析:
本题解析:
本题难度:一般
5、选择题 海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
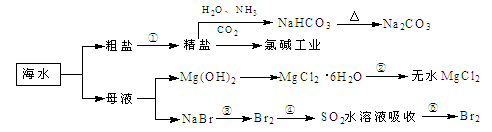
下列有关说法正确的是
A.过程①中除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.过程②中结晶出的MgCl2・6H2O要在HCl氛围中加热脱水制得无水MgCl2
D.工业上通过电解饱和MgCl2溶液制取金属镁
参考答案:C
本题解析:
试题分析:A、除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,错误;B、石灰水与NaHCO3和Na2CO3均反应,生成白色沉淀,不能鉴别,错误;C、MgCl2・6H2O水解生成氢氧化镁和氯化氢,加热促进水解,最终得氧化镁,所以为了抑制水解,要在HCl氛围中加热脱水制得无水MgCl2,正确;D、电解饱和MgCl2溶液得到氢氧化镁沉淀,得不到镁单质,错误,答案选C。
本题难度:一般