?
�ο��𰸣��� n (N2)="0" (1��)??? n (H2)="0
�����������1���ڱ��ֺ�ѹʱҪʹƽ���Ч���������Ͷ�ϵı�ֵ����ͬ�ģ����������֪����ĵ��������������֮����1�U4�ģ�����ͨ������ʽ�����ĵ��������������֮�ȱ�������1�U4����ʵ������谱�������ʵ�����x����xmol������������0.5xmol������1.5xmol��������һ����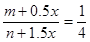 �����x��2(n-4m)mol��ƽ���ǵ�Ч�ģ����Ը������ʵĺ����ֱ�����ͬ�ģ�����ƽ��ʱ���������ʵ����Dz�ͬ�ġ����������ʵ�������ʼʱ���������ʵ��������ȡ� �����x��2(n-4m)mol��ƽ���ǵ�Ч�ģ����Ը������ʵĺ����ֱ�����ͬ�ģ�����ƽ��ʱ���������ʵ����Dz�ͬ�ġ����������ʵ�������ʼʱ���������ʵ��������ȡ�
�����Ѷȣ�һ��
2��ѡ���� ��֪2SO2(g)+O2(g)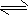 2SO3(g)����H=-197kJ/mol��ͬ���£�����ͬ������ܱ������ס����зֱ���� 2SO3(g)����H=-197kJ/mol��ͬ���£�����ͬ������ܱ������ס����зֱ����
2molSO2��1molO2��1molSO3��1molSO2��0.5molO2�������Ƿֱ�ﵽƽ��ʱ�ų�������ΪQ1KJ��Q2KJ�������бȽ���ȷ����[???? ]
A��Q2= 1/2 Q1=98.5
B��Q2=1/2 Q1<98.5
C��Q2<1/2 Q1<98.5
D��1/2 Q1< Q2 <98.5
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ij�¶��£���һ�ݻ��̶��������У���ӦaA��g��+bB��g��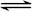 hH��g���ﵽƽ���A��B��H�����ʵ����ֱ�Ϊamol��bmol��hmol����֪a+b=2h�����������¶Ȳ��䣬�����ߵ����ʵ�������һ�����������ж���ȷ���� hH��g���ﵽƽ���A��B��H�����ʵ����ֱ�Ϊamol��bmol��hmol����֪a+b=2h�����������¶Ȳ��䣬�����ߵ����ʵ�������һ�����������ж���ȷ����
A��ƽ�ⲻ�ƶ�??????????? B�����������ܶȲ���
C��B�������������?????? D��amol/L��c��A����2amol/L
�ο��𰸣�C
����������������¶Ȳ��䣬�����ߵ����ʵ�������һ������ϵ�и���ֵ�Ũ��ͻ��Ϊԭ����2�������൱����ԭƽ��Ļ���������ѹǿ�����������Ϊԭ��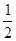 �����ԣ� �����ԣ�
A����ƽ�⽫������Ӧ�����ƶ���B�������������ܶ�����C��ȷ��D�������ڷ�ӦΪ���淴Ӧ����Ӧ�ﲻ����ȫת��Ϊ�����
�����Ѷȣ�һ��
4��ѡ���� ��һ���¶ȣ��̶�������ܱ������У������������ǿ��淴ӦA(g)+3B(g)? ?2C(g)�ﵽƽ���־���ǣ�???�� ?2C(g)�ﵽƽ���־���ǣ�???��
��C������������C�ķֽ�������ȣ��ڵ�λʱ������amol A��ͬʱ����3amolB����A��B��C��Ũ�Ȳ��ٱ仯����A��B��C��ѹǿ���ٱ仯���ݻ��������ܶȲ��ٱ仯�������������ʵ������ٱ仯���ߵ�λʱ������amol A��ͬʱ����2amol C����A��B��C�ķ�����Ŀ��Ϊ1:3:2�����������ƽ����Է����������ٱ仯????
A. �ڢݢ�???? B. �ߢ�?????? C. �٢�??????? D. �ݢޢ�
�ο��𰸣�A
���������
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0�����������ʵ�Ũ�Ȼ��������ٷ����仯��״̬���ǻ�ѧƽ��״̬�����Ԣ٢���ȷ�����з�Ӧ���ʵķ�������ͬ�ģ�����֮������Ӧ�Ļ�ѧ������֮�ȣ���ˢ��еĹ�ϵʼ���dz���������ȷ���÷�Ӧ�������С�Ŀ��淴Ӧ����ѹǿ�����ʵ���Ҳ�Ǽ�С�ģ����Ե�ѹǿ�����ʵ������ٷ����仯ʱ������˵�����ܢ���ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ��ݲ���ȷ�����з�Ӧ���ʵķ����෴��������������֮������Ӧ�Ļ�ѧ������֮�ȣ�����ȷ��ƽ��ʱŨ�Ȳ��ٷ����仯��������֮���Ũ�Ȳ�һ����Ȼ�����ij�ֹ�ϵ�����ȷ���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ���������䣬�����ʵ����DZ仯�ģ����Ԣ����˵������ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ����Ҫ�ǿ���ѧ���Կ��淴Ӧƽ��״̬���˽����ճ̶ȣ��Լ�������û���֪ʶ�ж�ƽ��״̬������������������ѧ���������������ͳ���˼ά���������ѧ����Ӧ��������ѧϰЧ�ʡ�����Ĺؼ�����ȷ���淴Ӧƽ��״̬�ĺ��壬�Լ��ж����ݣ����ܽ������������ü��ɡ�
�����Ѷȣ���
5��ѡ���� mA(g) + nB(g)  ?pC(g)��ͬһѹǿ�±仯��ͼ������������ȷ���� ?pC(g)��ͬһѹǿ�±仯��ͼ������������ȷ����
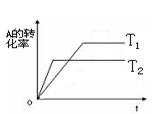
A��T1��T2����Ӧ�����ȷ�Ӧ
B��T1��T2����Ӧ�Ƿ��ȷ�Ӧ
C��T1��T2����Ӧ�����ȷ�Ӧ
D��T1��T2����Ӧ�Ƿ��ȷ�Ӧ
�ο��𰸣�B
�����������
�����Ѷȣ���
|