��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ܱ������У�ͨ��2 mol SO2��1 mol O2��������Ӧ2SO2+O2 2SO3����t1ʱ�̴ﵽƽ�⡣���������������䣬��t2ʱ�̣���ͨ��һ������SO3�������йط�Ӧ����(v)��ʱ��(t)�Ĺ�ϵ������ȷ����(?? )
2SO3����t1ʱ�̴ﵽƽ�⡣���������������䣬��t2ʱ�̣���ͨ��һ������SO3�������йط�Ӧ����(v)��ʱ��(t)�Ĺ�ϵ������ȷ����(?? )

�ο��𰸣�A
�����������Ӧ�ﵽƽ��ʱ������SO3��Ũ�ȣ�˲���淴Ӧ������������Ӧ���ʲ��䣬��A����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ���и�ͼ���ܱ�ʾA(g)+B(g)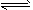 2C(g)������ӦΪ���ȷ�Ӧ��������淴Ӧ��ͼ��Ϊ
2C(g)������ӦΪ���ȷ�Ӧ��������淴Ӧ��ͼ��Ϊ
A��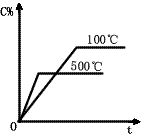
B��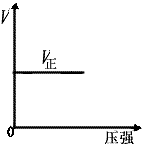
C��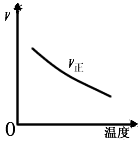
D��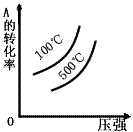
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ���ǣ� ��
A�������Է����еķ�Ӧ�������ȷ�Ӧ
B����ѧ������ʱ���յ��������ڻ�ѧ���γ�ʱ�ų��������ķ�Ӧ���ڷ��ȷ�Ӧ
C�����߷�Ӧ���¶ȣ�����Ӱٷ������ӣ����Ӽ���Ч��ײ�ļ�����ߣ���Ӧ��������
D������ͨ���ı䷴Ӧ·����ʹ��Ӧ�����������ı䷴Ӧ����Ļ��
�ο��𰸣�C
���������
���������A�������Է����еķ�Ӧ��һ���������ȷ�Ӧ������B����ѧ������ʱ���յ��������ڻ�ѧ���γ�ʱ�ų��������ķ�Ӧ�������ȷ�Ӧ������C�����߷�Ӧ���¶ȣ�����Ӱٷ������ӣ����Ӽ���Ч��ײ�ļ�����ߣ���Ӧ����������ȷ��D������ͨ���ı䷴Ӧ·����ʹ��Ӧ�������ı䷴Ӧ����Ļ�ܣ�����
���㣺���鷴Ӧ������ܡ��¶ȡ���ܵȹ�ϵ��֪ʶ��
�����Ѷȣ�һ��
4������� ��9�֣�ijС��ѧ�����о���ͬ���ʶ�˫��ˮ�ֽ����ʵ�Ӱ�죬������������50mLΪ�������������ʵ�鷽����
ʵ�����
| ˫��ˮ���
| ˫��ˮŨ��
| ���ӵ�����
| ��������X
|
1
| 100mL
| 20%
| ��
|
|
2
| 100mL
| 20%
| 10gMnO2
|
|
3
| 100mL
| 20%
| 10gKI
|
|
4
| 100mL
| 20%
| ��������
|
��1���ڸ��о������У�MnO2��KI��������˫��ˮ�ֽ�Ĺ����п����� �����á�
��2����������XΪ ��
��3�����´�ʩ���Լӿ��ʵ����˫��ˮ�ֽ����ʵ��ǣ� �����ţ���
A����˫��ˮ�����������200mL
B����˫��ˮ��Ũ��������30%
C����װ��A����
D�������ƶ�Bװ��ʹ������������ѹǿ����
��4���ӿ��Ʊ�����ԭ���������÷����Ƿ���� ����ǡ����������ǣ�
�ο��𰸣�����9�֣�����1�������������ı仯ѧ��Ӧ���ʻ�����ѧ
���������
�����������1����������������ͬ��ֻ�Ǽ����MnO2��KI�����β�ͬ������ڸ��о������У�MnO2��KI��������˫��ˮ�ֽ�Ĺ����п������������ã���2��˫��ˮ�ֽ�������������˴�������XΪ����50mL������Ҫ��ʱ�䣻��3������Ӱ�컯ѧ��Ӧ���ʵ�������Ũ�ȡ��¶ȣ������¶ȣ���ѧ��Ӧ���ʻ�ӿ죬����Ӧ���Ũ�ȣ���ѧ��Ӧ���ʼӿ죻����������μӵķ�Ӧ���е�ѹǿ����ѧ��Ӧ���ʻ�ӿ죻�����й���μӵķ�Ӧ����Ũ�Ȳ��䣬�����������Ӵ������Ӧ����Ҳ��ӿ졣�������������Լӿ��ʵ����˫��ˮ�ֽ����ʵ���B��C����4�� �ӿ��Ʊ�����ԭ���������÷�����������ԭ����2��3��������ʶ���10g,4��ʵ�����������ε�����Ӧѡ��10g������û�������Ķ��٣��ʲ�������
���㣺���黯ѧʵ�鷽������������ۡ�Ӱ�컯ѧ��Ӧ���ʵ����ص�֪ʶ��
�����Ѷȣ�һ��
5������� �α���ͨ������ᣨH2C2O4����Һ�еμ��������ữ����������о�Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬����д���÷�Ӧ�Ļ�ѧ����ʽ??????????????????????????????���÷�Ӧ����ʹ��ָʾ����ԭ����??????????????????????????��
��ijͬѧ���ݿα���������Ի�ѧ��Ӧ���ʵ�Ӱ��ԭ�����������������������ᷴӦ�й�ʵ�飬ʵ����̵����ݼ�¼���£����������ϱ�����Ϣ���ش��й����⣺
ʵ��
���
| ��Ӧ�¶�
���棩
| �μӷ�Ӧ������
| Na2S2O3
| H2SO4
| H2O
| V/mL
| c/mol?L-1
| V/mL
| c/mol?L-1
| V/mL
| A
| 20
| 10
| 0��1
| 10
| 0��1
| 0
| B
| 20
| 5
| 0��1
| 10
| 0��1
| 5
| C
| 20
| 10
| 0��1
| 5
| 0��1
| 5
| D
| 40
| 5
| 0��1
| 10
| 0��1
| 5
?
��1��д��������Ӧ�����ӷ���ʽ???????????????????????????
��2�������������յ�֪ʶ�жϣ�������ʵ���з�Ӧ�������Ŀ�����?????����ʵ����ţ�
��3�������ñȽ�ijһ���ض�ʵ�������Ӱ��ʱ�������ų��������صı䶯���ţ�����Ҫ���ƺ���ʵ����??�صĸ��Ӧ���������У�
����˵���¶ȶԸ÷�Ӧ����Ӱ�����ϱȽ���?????������ʵ����ţ�
��A��B��A��C����ϱȽ����о���������??????????????????????????
��B��C����ϱȽ����о���������????????????????????????????????
��4���̲��������˳��ֻ�ɫ�����Ŀ������ȽϷ�Ӧ���ʵĿ������������Ϊ�β�������ˮ��������λʱ������������Ĵ�С�Ŀ���ԭ��???????????????????????????????????
�ο��𰸣���5H2C2O4+3H2S04+2KMnO4=K2SO4+
���������
���������������ᣨH2C2O4����Һ�еμ��������ữ������صĻ�ѧ����ʽΪ��5H2C2O4+3H2S04+2KMnO4=K2SO4+2MnSO4+10CO2+8H2O������Ϊ���������Һ�淴Ӧ�Ľ�������ɫ�ı仯���ʸ÷�Ӧ����ʹ��ָʾ������1�������������Ӻ������ӷ�Ӧ�������������ˮ�����ӷ�Ӧ����ʽΪ��S2O32-+2H+�TS��+SO2+H2O����2���¶�Խ�ߣ���Ӧ����Խ�죬Ũ��Խ��Ӧ����Խ�죬������ʵ���з�Ӧ�������Ŀ�����D����3������˵���¶ȶԸ÷�Ӧ����Ӱ�����������ߵ��¶Ȳ�
�����Ѷȣ�һ��
|
|