微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)在一个固定体积为2升的密闭容器中,充入2 mol A和1 mol B,发生如下反应:2A(g)+B(g)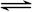 3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
(1) 写出该反应平衡常数的表达式_____________________,2分钟内B 的平均反应速度为_____________________;
(2) 若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为______(填“吸热”或“放热”)反应;
(3) 若将容器体积缩小至1升,反应达到平衡时C的浓度为___________mol/L,平衡常数___________ (填“增大”、“减小”或“不变”)。
参考答案:(1)K=[C(C)] 3/[C(A)] 2?[C(B)]?
本题解析:(1)平衡常数是指当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂
之积的比值,所以该反应的平衡常数表达式为K=[C(C)] 3/[C(A)] 2?[C(B)]。C的浓度为1.2 mol/L,则消耗B的浓度是0.4mol/L,所以反应速率是0.4mol/L÷2min=0.2mol/(L?min)。
(2)使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,由于反应前后体积不变,但质量是变化的,这说明平衡向正反应方向进行,因此正反应是吸热反应。
(3)由于反应前后体积不变,所以改变压强平衡不移动。但浓度都变为用来的2倍,即C的浓度是2.4mol/L。平衡常数只与温度有关系,所以平衡常数不变。
本题难度:一般
2、填空题 (8分)
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①3种溶液中,物质的量浓度最大的是________。
②分别用0.1 mol・L-1的NaOH溶液中和,其中消耗NaOH溶液最多的是________。
③与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快
B.H2SO4最快
C.CH3COOH最快
D.一样快
参考答案:(1)③???(2)①CH3COOH??②CH3COOH??
本题解析:(1)碳酸钠和盐酸反应是分步进行的,即Na2CO3+HCl=NaHCO3+NaCl、NaHCO3+HCl=NaCl+H2O+CO2↑,所以答案选③。
(2)①盐酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,所以在pH相等的条件小,醋酸的浓度大。
②醋酸浓度大,则消耗的氢氧化钠也多。
③反应开始时,氢离子浓度是相同的,所以反应速率相同,答案选D。
本题难度:一般
3、选择题 在一定温度下将1mol CO和3mol水蒸气放在密闭的容器中发生下列反应:
CO(g)+H2O(g)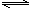 CO2(g)+H2(g)
CO2(g)+H2(g)
达到平衡后,测得 CO2为0.75mol,再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和为 [???? ]
A.1.2mol
B.1.5mol
C.1.8mol
D.2.5mol
参考答案:C
本题解析:
本题难度:一般
4、选择题 在恒温下的密闭容器中,有可逆反应2NO(g)+O2(g) 2NO2(g),不能说明该反应已达到平衡状态的是(?????? ) ??????????????????????????????????????????????
2NO2(g),不能说明该反应已达到平衡状态的是(?????? ) ??????????????????????????????????????????????
A.混合气体的颜色不再变化
B.反应器中的压强不随时间的变化而变化
C.混合气体中NO2的体积分数保持不变
D.生成NO2的速率与生成O2的速率相等
参考答案:D
本题解析:颜色不再变化,即说明浓度不再变化,A可以。反应前后体积是变化的,即压强是变化的,当压强不再变化时,可以说明。物质当体积分数不再变化,即说明反应已经达到平衡状态。选项D中当反应速率方向相反,但不满足速率之比是相应但化学计量数之比,即正逆反应速率不相等,所以不能说明。答案选D。
本题难度:一般
5、选择题 已知2SO2(g)+O2(g)  ?2SO3 (g)?△H =-a kJ・mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放出热量x kJ
?2SO3 (g)?△H =-a kJ・mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放出热量x kJ
下列判断正确的是(????? )
A.反应放出热量x="0.05" a
B.反应达到平衡状态时,2v (SO2)消耗=" v" (O2) 生成
C.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,平衡后反应放出的热量y kJ,则y < x
D.升高温度,平衡常数变小
参考答案:D
本题解析:
试题分析:A、恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,可逆反应不可能进行到底,放出的热量小于0.05 a ,错误;B、反应达到平衡状态时,v (SO2)消耗="2" v (O2)生成,错误;C、,在恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,压强减小,反应放出热量x kJ,若保持恒温恒压,需要缩小体积,回复到原来的压强,相当于增大压强,平衡向正反应方向移动,则y>x,错误;D、因为是放热反应,升高温度,平衡常数变小,正确。
本题难度:一般