微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏加德罗常数,下列叙述不正确的是
A.标准状况下,22.4L H2含有的分子数为 NA
B.常温常压下,14g N2含有分子数为0.5NA
C.2.3g金属钠做还原剂时失去的电子数为0.1NA
D.物质的量浓度为0.5mol /L的MgCl2溶液中,含有Cl-个数为NA
参考答案:D
本题解析:D不正确,不知道溶液的体积,无法计算物质的量;
本题难度:一般
2、选择题 设NA为阿伏加德罗常数,下列说法中正确的是:
A.在常温常压下,11.2 L氮气所含有的原子数目为NA
B.活泼金属从盐酸中置换出1 mol H2,电子转移数为NA
C.500 mL 0.5mol/L Al2(SO4)3溶液中,SO42-的浓度为1.5 mol・L-1
D.1.7 g氨气所含的电子数目为 10 NA
参考答案:C
本题解析:考查气体的摩尔体积;
A.常温常压下,11.2 L氮气并非0.5mol,故所含原子无法计算
B.由2H+-2e-=H2↑可知,每得到1 mol H2,电子转移数为2NA
C.正确
D.1.7 g氨气所含的电子数目为: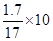 NA
NA
本题难度:一般
3、填空题 (6分)乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。

利用标签提供的信息,回答下列问题:
(1)乙酸的摩尔质量为 。
(2)若该乙酸溶液的密度为1.02g/cm3,求此乙酸溶液的物质的量浓度。(写出计算过程,结果精确到0.01)
(3)用此酸配制250mL2mol/L的稀乙酸,需要这种乙酸的体积是多少。(写出计算过程)
参考答案:(1)60g/mol;(2)根据质量分数与物质的量浓度的换算
本题解析:
试题分析:(1)乙酸的摩尔质量在数值上等于其相对分子质量,其相对分子质量为12×2+1×4+16×2=60,则摩尔质量为60g/mol。(2)根据质量分数与物质的量浓度的换算公式,c=1000×密度×质量分数/摩尔质量,进行计算,c=1000×1.02×36%/60=6.12mol/L。(3)根据溶液的稀释过程中溶质的物质的量相等,即公式c1v1=c2v2,则250×2=6.12×v 计算得v=81.7ml。
考点:摩尔质量,物质的量浓度与质量分数的换算,溶液的稀释。
本题难度:一般
4、简答题 实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液.为确定甲、乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取25.00mL甲溶液,向其中缓慢滴加乙溶液15.00mL,共收集到二氧化碳气体224mL.
②另取15.00mL乙溶液,向其中缓慢滴加甲溶液25.00mL,共收集到二氧化碳气体112mL.
上述气体体积均已换算为标准状况,则根据上述操述及实验数据填空:
(1)写出操作①所涉及反应的离子方程式______;
(2)甲溶液的物质的量浓度为______,乙溶液的物质的量浓度为______;(二氧化碳在溶液中的少量溶解忽略不计)
(3)将n?mL的甲溶液与等体积的乙溶液按各种可能的方式混合,产生的气体体积为V?mL(标准状况),则V的取值范围为______.
参考答案:(1)若将Na2CO3溶液滴入盐酸溶液,则盐酸相对过量,所有
本题解析:
本题难度:一般
5、选择题 用NA代表阿佛加德罗常数,下列说法正确的是
A.360g C60晶体中的分子数为NA
B.标况下,11.2L SO3所含的分子数目为0.5NA
C.0.1mol/L稀硫酸中含SO42-离子个数为0.1NA
D.0.1mol CH5+所含的电子数目为NA
参考答案:D
本题解析:考查阿伏加德罗常数的有关计算与判断。碳-60的相对分子质量是720,所以选项A中含有0.5NA个分子,A不正确;标准状况下,三氧化硫不是气体,不能适用于气体摩尔体积,选项B不正确;选项C不正确,因为不能确定溶液的体积,因此正确的答案选D。
本题难度:一般