微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)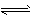 2NH3(g)△H= -92.4 kJ/mol]:
2NH3(g)△H= -92.4 kJ/mol]:

下列说法正确的是[???? ]
A.2c1>c3
B.a+b =92.4
C.2P2
D.α1+α3<1
参考答案:BD
本题解析:
本题难度:一般
2、选择题 下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是?

参考答案:BD
本题解析:增大压强,A中平衡向正反应方向移动,B中平衡向正反应方向移动,C中平衡不移动,D中平衡向逆反应方向移动;升高温度,A中平衡向逆反应方向移动,B中平衡正反应方向移动,C中平衡向逆反应方向移动,D中平衡向逆反应方向移动,因此答案选BD。
本题难度:一般
3、选择题 说明可逆反应A(g)+B(g) C(g)+D(g)在一定条件下已达到化学平衡状态的事实是。??????????????????????
C(g)+D(g)在一定条件下已达到化学平衡状态的事实是。??????????????????????
A.容器内压强不随时间的变化而变化? B.容器内A、B、C、D四者共存
C.A、D的消耗速率相等????????????? D.C、D的生成速率相等
参考答案:C
本题解析:略
本题难度:简单
4、选择题 在不同情况下测得A(g)+3B(g)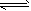 2C(g)+2D(g)的下列反应速率,其中反应速率最大的是 [???? ]
2C(g)+2D(g)的下列反应速率,其中反应速率最大的是 [???? ]
A.υ(D)=0.4 mol・L-1・s-1
B.υ(C)=0.5 mol・L-1・s-1
C.υ(B)=0.6 mol・L-1・s-1
D.υ(A)=0.15 mol・L-1・s-1
参考答案:B
本题解析:
本题难度:简单
5、填空题 在100℃时,将0.200 mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下表格:
时间
| 0
| 20
| 40
| 60
| 80
| 100
|
c(N2O4)
| 0.100
| c1
| 0.050
| c3
| a
| b
|
c(NO2)
| 0.000
| 0.060
| c2
| 0.120
| 0.120
| 0.120
试填空:
(1)该反应的化学方程式为_________________________________,达到平衡时四氧化二氮的转化率为________%。
(2)20s时四氧化二氮的浓度c1=________mol・L-1,在0~20s时间段内,四氧化二氮的平均反应速率为________mol?L-1?s-1。
(3)若在相同情况下最初向容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的初始浓度为________mol?L-1。
参考答案:(1)N2O4 本题解析: 本题解析:
试题分析:(1)根据表中数据可知,N2O4是反应物,NO2是生成物,所以该反应的化学方程式为N2O4 2NO2。平衡时NO2的浓度是0.120mol/L,则根据方程式可知消耗N2O4的浓度是0.120mol/L÷2=0.060mol/L,因此NO2的转化率是 2NO2。平衡时NO2的浓度是0.120mol/L,则根据方程式可知消耗N2O4的浓度是0.120mol/L÷2=0.060mol/L,因此NO2的转化率是 。 。
(2)(2)20s时NO2的浓度是0.060mol/L,则消耗N2O4的浓度是0.030mol/L,所以四氧化二氮的浓度c1=0.100mol/L-0.030mol/L=0.070mol/L。则在0~20s时间段内,四氧化二氮的平均反应速率为0.030mol/L÷20s=0.0015_mol?L-1?s-1。
(3)由于N2O4的最初浓度是0.100mol/L,完全转化为NO2时,NO2的浓度应该是0.200mol/L,所以若在相同情况下最初向容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的初始浓度为0.200mol/L。
点评:该题是中等难度的试题,试题基础性强,难易适中,侧重对学生基础知识的巩固与训练,有助于培养学生的应试能力,提高学生的学习效率。该题的难点是等效平衡的判断和应用,学生需要明确的是所谓等效平衡是指外界条件相同时,同一可逆反应只要起始浓度相当,无论经过何种途径,都可以达到相同的平衡状态。等效平衡的判断及处理一般步骤是:进行等效转化――边倒法,即按照反应方程式的计量数之比转化到同一边的量,与题干所给起始投料情况比较即可。
本题难度:一般
|