微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 氯气、液氯、盐酸、氯水中均含有
A.氯分子
B.氯原子
C.氯离子
D.氯元素
参考答案:D
本题解析:此类题选择防毒的合适物质必须考虑三个方面:一是要能够吸收氯气;二是本身无毒、无腐蚀性,对人体无害;三是吸收氯气时生成的产物也应对人体无害。
本题难度:困难
2、选择题 钠着火时,可用来灭火的物质或器材是
A.水
B.干冰
C.沙子
D.泡沫灭火器
参考答案:C
本题解析:分析:金属钠是一种活泼金属,用来灭火的物质和金属钠以及钠燃烧后的产物也不反应.
解答:A、金属钠和水之间能反应,不能用水灭火,故A错误.
B、钠燃烧后的产物过氧化钠能与二氧化碳反应产生氧气,使燃烧加剧,故B错误;
C、沙子不易燃,能将金属钠和空气隔离,起到灭火的作用,故C正确;
D、钠燃烧后的产物过氧化钠能与二氧化碳反应产生氧气,使燃烧加剧,故D错误;
故选:C.
点评:本题考查学生金属钠以及过氧化钠的性质和灭火的原理知识,可以根据所学知识进行回答,难度不大.
本题难度:困难
3、选择题 取不同质量的镁铝合金分别与25mL同浓度的稀硝酸反应,测量合金的质量与产生气体的体积(标准状况),列表如下:
A.A
B.B
C.C
D.D
参考答案:AD
本题解析:分析:分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为224mL×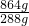 =672mL>560mL,故第3组金属有剩余,硝酸完全反应.
=672mL>560mL,故第3组金属有剩余,硝酸完全反应.
第3个实验后向反应容器内加入足量的1.0mol/L?NaOH(aq)充分反应,使固体质量不再发生变化,使氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2.
根据n=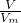 计算第3组生成的NO的物质的量,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的
计算第3组生成的NO的物质的量,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的 ,据此计算25mL硝酸溶液中n(HNO3)、起酸性作用的硝酸的物质的量,根据c=
,据此计算25mL硝酸溶液中n(HNO3)、起酸性作用的硝酸的物质的量,根据c=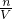 计算原硝酸溶液的浓度;
计算原硝酸溶液的浓度;
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,根据二者质量与转移电子数目列方程计算x、y的值,进而计算864mg合金中Al的物质的量,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2),再根据V= 计算需要氢氧化钠溶液的最小体积.
计算需要氢氧化钠溶液的最小体积.
解答:分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为224mL×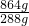 =672mL>560mL,故第3组金属有剩余,硝酸完全反应.
=672mL>560mL,故第3组金属有剩余,硝酸完全反应.
第3个实验后向反应容器内加入足量的1.0mol/L?NaOH(aq)充分反应,使固体质量不再发生变化,使氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2.
第3组生成的NO的物质的量为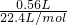 =0.025mol,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的
=0.025mol,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的 ,故25mL硝酸溶液中n(HNO3)=0.025mol÷
,故25mL硝酸溶液中n(HNO3)=0.025mol÷
=0.1mol,原硝酸溶液的浓度为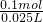 =4mol/L.
=4mol/L.
起酸性作用的硝酸的物质的量为0.1mol-0.025mol=0.075mol,
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,由二者质量与转移电子数目守恒有:
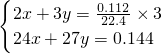
解得x=0.0015,y=0.004,
故864mg合金中Al的物质的量0.004mol×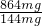 =0.024mol,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为
=0.024mol,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为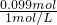 =0.099L=99mL,
=0.099L=99mL,
故选AD.
点评:本题考查混合物的有关计算,过程复杂、计算量较大,题目难度较大,注意利用守恒思想进行的解答.
本题难度:困难
4、选择题 已知NaCN溶液呈碱性;(CN)2与卤素单质的性质相似;CN-的还原性介于Br-、I-之间.下列变化不能发生的是
A.HCN?H++CN-
B.(CN)2+CH2=CH2→NC-CH2-CH2-CN
C.(CN)2+2Br-→2CN-+Br2
D.(CN)2+2OH-→CN-+CNO-+H2O
参考答案:C
本题解析:分析:A.NaCN溶液呈碱性,说明HCN羧基弱酸,存在电离平衡;
B.(CN)2与卤素单质的性质相似,可以与乙烯发生加成反应;
C.满足还原剂的还原性强于还原产物的还原性,反应可能发生;
D.(CN)2与卤素单质的性质相似,可以发生类似氯气与碱的反应.
解答:A.NaCN溶液呈碱性,说明HCN羧基弱酸,存在电离平衡,电离方程式为HCN?H++CN-,故A正确;
B.(CN)2与卤素单质的性质相似,可以与乙烯发生加成反应生成NC-CH2-CH2-CN,故B正确;
C.由题目信息可知,还原性CN->Br-,Br-不能还原(CN)2为CN-,故C错误;
D.(CN)2与卤素单质的性质相似,可以发生类似氯气与碱的反应,与碱发生反应(CN)2+2OH-=CN-+CNO-+H2O,故D正确;
故选C.
点评:本题考查类卤素知识、氧化还原反应、盐类水解等,需要学生对信息应用进行利用,注意把握题中信息,“类卤素”与卤素单质的性质相似,是高考热点题型.
本题难度:一般
5、选择题 下列物质的化学名称、化学式、和俗名一致的是
A.碳酸钠、Na2CO3、苏打
B.碳酸钙、CaCO3、生石灰
C.氢氧化钠、NaOH、纯碱
D.碳酸氢钠、NaHCO3、苏打
参考答案:A
本题解析:分析:根据常见化学物质的名称、俗称、化学式进行分析判断即可.
解答:A、碳酸钠、Na2CO3、苏打,化学名称、化学式、和俗名一致,故A正确;
B、碳酸钙、CaCO3化学名称、化学式一致,生石灰是氧化钙,不是碳酸钙的俗称,故B错误;
C、氢氧化钠、NaOH化学名称、化学式一致,纯碱是碳酸钠,属于盐不是氢氧化钠的俗称,故C错误;
D、碳酸氢钠、NaHCO3化学名称、化学式一致,俗称为小苏打,故D错误;
故选A.
点评:本题难度不大,熟练掌握常见化学物质的名称、俗称、化学式是正确解答此类题的关键.
本题难度:困难