��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������������������NH3����
A��Ũ����
B����ʯ��
C��AlCl3��Һ
D��ʳ��ˮ
�ο��𰸣�B
��������������Ǽ������壬��������ˮ������ֻ���ü�ʯ�Ҹ����ѡB��
�����Ѷȣ���
2��ʵ���� ��3a L NO2��������ͨ��ʢ���������ʵ�����������NaHCO3��Һ��Ũ���ᡢ����Na2O2��������Ӧ�Ļ�ѧ����ʽ�ǣ�1��________����2��________����3��________���������ˮ���ռ��������壬�ռ�����������________�������________L��
�ο��𰸣���1��3NO2+2H2O�T�T2HNO3+ NO
��2��
��������������Ļ�ѧ��Ӧ�ķ���ʽ�ǣ�1��3NO2+2H2O�T�T2HNO3+ NO
��2�� HNO3+ NaHCO3�T�TNaNO3+H2O+ CO2
��3��2Na2O2+2CO2�T�T2Na2CO3+O2
�ɷ���ʽ�ɿ�����3NO2��2HNO3��2 CO2��O2??? 3 NO2��NO
3a L????????????? a L??? 3a L? a L
��ˮ���ռ���4NO+3 O2+2H2O�T�T4HNO3
a L? a L
�ɷ���ʽ��֪��O2ʣ��0.25a L
�����Ѷȣ���
3��ʵ���� ��17�֣���ѧ������3.0 mol��L-1ϡ������̽����ʵ�飬����ʱʵ����ֻ��18.4 mol��L-1Ũ���ᡣ����Ϊ������100 mL 3.0 mol��L-1ϡ���ᡣ
��1)�������ƹ������£�
�ټ�������Ũ����������????????(ȷ��С�����һλ)����ȡŨ�������õ���Ͳ�Ĺ����???����������ѡ��A.10 mL��B.25 mL��C.50 mL��D.100 mL����
��ϡ�͡��������������??????????????????????????????????????????��
�۴��ϲ��õ���ϡ��Һ�����ȴ����������������ע��?????????��������ˮϴ���ձ��ڱںͲ�����2-3�Σ�ϴ��ҺҲע�����С�����ҡ������ƿ��ʹ��Һ��Ͼ��ȡ�
�ܽ�����ˮע������ƿ����Һ��������ƿ�̶���1-2cm������?????��ˮ��Һ����̶������С��Ǻ�ƿ�����������µߵ���ҡ�ȡ�
�ݽ���õ���Һת�Ƶ��Լ�ƿ�У�����ͬѧʹ�á�
��2����������Һ�����У������������ʱ��ʵ��Ũ�Ȼ�����������ƫ�ߡ�ƫ�ͻ�Ӱ�죩
A.���õ�Ũ���᳤ʱ��������ܷⲻ�õ�������????????????
B.����ƿ������ˮϴ�Ӻ������������ˮ????????????
C.���ù����ձ���������δϴ��?????????????
D.����ʱ���ӿ̶���?????????????
�ο��𰸣�16.3mL? B��25mL��1�֣�����ÿ��2�֣�??��װ��
���������
�����������1��1����Ũ��������ΪV��18.4mol/L��V=0.1L��3.0mol/L��V=0.0163L=16.3mL��ѡȡ��Ͳ���ݻ�Ӧ�Դ��ڻ������ȡ��Һ���������ѡB��
�ʴ�Ϊ��16.3ml��B��
Ȼ��Ũ�������ձ��ڱڻ��������ձ��У����ò��������裬��ֹҺ��ɽ���
�ʴ�Ϊ����װ��ˮ���ձ��ڱڻ���ע��Ũ���ᣬ�ӱ߽��裻
3��ϴ��ҺҪת�Ƶ�100mL����ƿ�У��ʴ�Ϊ��100mL����ƿ��
4��������ˮע������ƿ����Һ��������ƿ�̶���1-2cm������ ��ͷ�ιܼ�ˮ��Һ����̶������У��Ǻ�ƿ�����������µߵ���ҡ�ȡ�
�ʴ�Ϊ����ͷ�ιܣ�
��2��A�����õ�Ũ���᳤ʱ��������ܷⲻ�õ������У�Ũ��������ˮ�ԣ��������ʵ����ʵ���ƫС��������Һ��Ũ��ƫ�ͣ�
B������ƿ������ϴ�Ӻ������������ˮ����Ӱ�����ʵ����ʵ�������Һ�����������������Һ�����ʵ���Ũ����Ӱ�졣
C�����ù����ձ���������δϴ�ӣ��������ʵ����ʵ���ƫС�����Ƶ���ҺŨ��ƫ�ͣ�
D������ʱ������Һ��Һ���棬������Һ�����ƫС������������Һ��Ũ��ƫ�ߡ�
�ʴ�Ϊ��ƫ�ͣ���Ӱ�죻ƫ�ͣ�ƫ�ߣ�
���������⿼����һ�����ʵ���Ũ����Һ�����ƣ��ѶȲ��������ȡŨ��������ѡ����Ͳ
�����Ѷȣ�һ��
4������� 
 (9��)��֪NH3��CuO�ڼ��������¿�����N2������ʽΪ2NH3��3CuO3Cu��N2��3H2O����������þ�ڸ����·�Ӧ�ɵõ�����þ������þ��ˮ��Ӧ������������þ�Ͱ�����
(9��)��֪NH3��CuO�ڼ��������¿�����N2������ʽΪ2NH3��3CuO3Cu��N2��3H2O����������þ�ڸ����·�Ӧ�ɵõ�����þ������þ��ˮ��Ӧ������������þ�Ͱ�����


(1)�����ǻ�ѧ����С���ͬѧ�����ʵ�����Ʊ������ļ��ַ�����
A������粒�������ʯ�ҹ���
B��Ũ��ˮ��μӵ����Ƶ���ʯ����
C����һ�������£���������������
D�����ȷֽ��Ȼ�粒���
����Ϊ���нϼ����еķ�����________________(����ĸ)���䷴Ӧ�Ļ�ѧ����ʽΪ��___________________________��___________________________��
(2)��С��ͬѧ��Ƶ��Ʊ�����þ��ʵ�鷽������ͼ (�гּ���������û�л���)������ʵ��ǰϵͳ�ڵĿ��������ž���
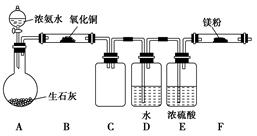
�ٸ�ʵ����ɺ��ܷ�õ������ĵ���þ________(��ܡ����ܡ�)����������____________________________________________________��
��װ��C��������___________________________________.
�ο��𰸣�(1)AB��(NH4)2SO4��Ca(OH)2CaSO4��2
�����������
�����Ѷȣ�һ��
5��ʵ���� ��12�֣����������(NH4)2SO4?FeSO4?6H2O��һ����Ҫ��ѧ�Լ���ʵ�����ó�ȥп�Ʋ����Ƭ����ȡ��������泥��������£�
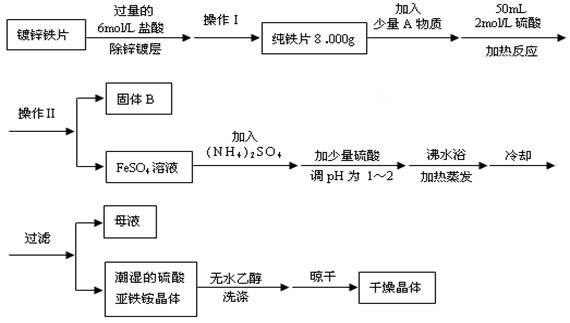
��ش��������⣺
��1��ȷ��п�Ʋ㱻��ȥ�ı�־��?????????????????????????��
����������Ƭп�Ʋ�ĺ�ȣ�����Ҫ��������????????????�����ţ���
a��п���ܶȦѣ�g/cm3��????? b����п��Ƭ����m 1��g��?? c������Ƭ����m 2��g��
d����п��Ƭ���S��cm2��??? e����п��Ƭ���h��cm��
��2�����������У���������ȡ����Ƭ��???????��????????��������
��3��A���ʿ���Ϊ????????�����ţ���
a��CuCl2?????? b��CuO?????? c��Cu(NO3)2?????? d��CuSO4??
��4������ˮ�Ҵ�ϴ�ӳ�ʪ����������茶�����Ϊ�˳�ȥ������������ˮ�֣����ü��Ⱥ�ɵ�ԭ����???????????????????��
��5���������þ����к���Fe2����NH4����SO42�����ӵ�ʵ�鷽����ȷ����?????�����ţ���
a��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬ͨ������Cl2���ټ�KSCN��Һ���۲�����
b��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬����NaOH��Һ��¶���ڿ����У��۲�����
c��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬����ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�����Թܿڣ��۲���ֽ��ɫ�ı仯
d��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬����������ټ���BaCl2��Һ���۲�����
�ο��𰸣���12�֣���1����Ӧ����ͻȻ��С������Ƭ�������ɵ�����ͻȻ��
�����������1�������������û�����������п�Ľ������Խ���ǿ���ʵ���Ƭ�������ɵ�����ͻȻ����ʱ������п�Ʋ��ѱ���ȥ
п�������Ϊ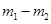 �������Ϊ
�������Ϊ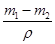 ������п��Ϊ���棬��п����Ϊ
������п��Ϊ���棬��п����Ϊ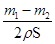 ���ʼ���п�Ʋ�ĺ�Ȳ���Ҫ����п��Ƭ��ȡ�
���ʼ���п�Ʋ�ĺ�Ȳ���Ҫ����п��Ƭ��ȡ�
��2������I��Ϊ�����ʵ�龫�ȣ����뽫��Ƭ����ϴ�Ӹɾ����ٸ�������
��3������ԭ��ط�Ӧ���ʿ��ڻ�ѧ��Ӧ��ͬʱΪ���������ʣ��ʿ�ͨ������CuO��CuSO4�γ���ͭԭ��أ��Լӿ췴Ӧ����
B�����ǹ����������û���ͭ
��4�����ڲ�Ʒ�ֽⲢ���ױ��������ʾ���������
��5��a����ʹ������Fe2+������Ҳ�ɳ���Ѫ��ɫ������ȷ
b��ͨ�����ɰ�ɫ������������ɫ�ı仯���ɼ����Fe2+�Ĵ��ڣ���ȷ
c:�����ݳ�����ֽ��ɫ��������ȷ
d�����Լ����SO42�D���ӵĴ��ڣ���ȷ
�����Ѷȣ�һ��