��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����л�ѧ����ʽ��д�����ӷ���ʽ����ȷ���� [???? ]
A. BaCO3+2HCl=BaCl2+CO2��+H2O,CO32-+2H+=CO2��+H2O
B. 2NaOH+H2SO4=Na2SO4+2H2O,H++OH-=H2O
C. Cu+2AgNO3=2Ag+Cu(NO3)2,Cu+Ag+=Cu2++Ag
D. H2SO4+Ba(OH)2 =BaSO4��+2H2O, H++OH-+Ba2++SO42- =BaSO4��+H2O
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A����������������������Һ��Ӧ��
CH3COOC2H5+OH�� �� CH3COOH+ C2H5O-
B����������Һ������ȩ��ȩ����
CH3CHO +2Ag(NH3)2+OH-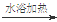 CH3COO- + NH4+ +3NH3 + 2Ag��+ H2O
CH3COO- + NH4+ +3NH3 + 2Ag��+ H2O
C��������Һ��ͨ��������CO2��
CO2 + H2O + 2C6H5O- 2C6H5OH + 2CO32-
2C6H5OH + 2CO32-
D���ʰ���������������Һ��Ӧ��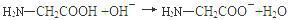
�ο��𰸣�D
���������A �������ɵ�����������Ӻ��Ҵ�
B ����������ҺӦд��������ʽ
C ���õ�����̼��������ӣ�����̼�������
D ��ȷ��
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A��̼��þ���������У�CO32-+2H+�TH2O+CO2��
B��AlCl3ˮ�ⷴӦ��Al3++3H2O�TAl��OH��3��+3H+
C����ϡ��ˮ�м���ϡ���NH3?H2O+H+�TNH4++H2O
D������ˮ�ⷴӦ��CO32-+2H2O?H2CO3+2OH-
�ο��𰸣�A��̼��þ���������е����ӷ�ӦΪMgCO3+2H+�TH2O+
���������
�����Ѷȣ���
4������� ���Ȼ�����Һ�Ʊ�����Ļ�ѧ����ʽΪ_______________________________��
�ο��𰸣�FeCl3+3H2O �����������
�����������
�����Ѷȣ���
5������� �����֣�ʳ���еĿ�����������軯�أ��仯ѧʽΪK4[Fe(CN)6]��3H2O��42.2 g K4[Fe(CN)6]��3H2O��Ʒ������ˮ���̵���������(��Ʒ�������¶ȵı仯����)����ͼ��ʾ��
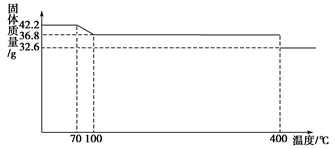
�Իش��������⣺
(1)��ȷ��150 ��ʱ�������ʵĻ�ѧʽ_____________��
(2)��������֪����Ȼ�����軯���������Ժܵͣ�����ˮ��Һ���ᷴӦ�ų��������軯��(HCN)���壻�����軯�ؼ�����һ���¶�ʱ�ֽܷ�����軯��(KCN)���ݴ��жϣ����ʳƷʱӦע�������Ϊ_____________________________________________________��
(3)��Fe2����Fe3���Ĵ������£���ʵ��2SO2��O2��2H2O��2H2SO4��ת������֪����SO2�ķ���ͨ�뺬Fe2����Fe3������Һ��ʱ������һ����Ӧ�����ӷ���ʽΪ4Fe2����O2��4H����4Fe3����2H2O������һ����Ӧ�����ӷ���ʽΪ__________________________��
(4)��֪Fe(OH)3���ܶȻ�����Ksp��1.1��10��36������ʱ��FeCl3��Һ�еμ�NaOH��Һ������ҺpHΪ3ʱ��ͨ������˵��Fe3���Ƿ������ȫ_____________��(��ʾ����ij����Ũ��С��10��5 mol��L��1ʱ������Ϊ�����ӳ�����ȫ)
�ο��𰸣�(ÿ�գ��֣���ͬ�����8��)(1)K4[Fe(CN)6]<
���������
�����������1��42.2 g K4[Fe(CN)6]��3H2O���ʵ�����42.2g��422g/mol��0.1mol�����нᾧˮ�����ʵ�����0.3mol��������0.3mol��18g/mol��5.4g������ͼ���֪����Ӧ���е�150��ʱ������ٵ�������42.2g��36.8g��5.4g����˵����ʱ���ٵ��������ǽᾧˮ����������˹���Ļ�ѧʽΪK4[Fe(CN)6]��
��2�����������軯��ˮ��Һ���ᷴӦ�ų��������軯��(HCN)���壬�������軯�ؼ�����һ���¶�ʱ�ֽܷ�����軯��(KCN)��������ʹ��
�����Ѷȣ�һ��