微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 黄铜矿主要成分是二硫化亚铁铜(CuFeS2)。黄铜矿经熔炼、煅烧后得到粗铜和炉渣,冶炼过程的主要反应有:
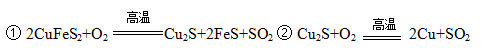
(1)二硫化亚铁铜也可以表示为CuS・FeS,其中硫元素的化合价是????。
(2)反应②中还原剂是????????。
(3)某校学习小组用炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)制备铁红,进行如下实验。
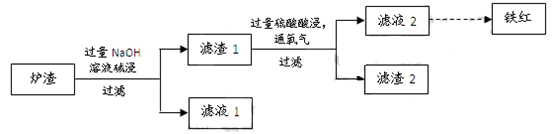
① 炉渣碱浸时反应的离子方程式是?????、?????。
② 滤渣1中加入硫酸并通入氧气可使FeO转化为Fe3+,该反应的离子方程式是????????;为检验铁元素是否被氧化完全,应进行的实验是:取少量滤液2于试管中?????????。
参考答案:(1)-2
(2)Cu2S
(3)①SiO2+2
本题解析:(1)二硫化亚铁铜也可以表示为CuS。FeS,其中硫元素的化合价是-2价;
(2)反应②中Cu2S中Cu元素的化合价由+1价升高到+2价,硫元素的化合价由-2价升高到+4价,被氧化,做还原剂;
(3)①炉渣中加入过量氢氧化钠溶液发生的离子方程式是SiO2+2OH-=SiO32-+H2O,Al2O3+2OH-=2AlO2-+H2O;②滤渣1中加入硫酸并通入氧气可使FeO转化为Fe3+,该反应的离子方程式是,4FeO+O2+12H+=4Fe3++6H2O;为检验铁元素是否被完全氧化,可难舍难分滤液
本题难度:一般
2、选择题 下列说法正确的是( )
A.由于水分子之间存在氢键,所以水分子比较稳定
B.晶体中有阴离子则必然有阳离子,有阳离子一定有阴离子
C.NH4HSO3溶液与足量NaOH溶液混合加热:NH4++HSO3-+2OH-
??△??
.
?
NH3↑+SO32-+2H2O
D.电解水生成H2和O2的实验中,可加入少量盐酸或硫酸增强导电性
参考答案:A.由于水分子之间存在氢键,则水的沸点高,其稳定性与化学键有
本题解析:
本题难度:简单
3、选择题 下列离子反应方程式正确的是? [???? ]
A.用两个铜电极电解食盐水:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑
B.腐蚀法制作印刷线路板:Fe3+ +Cu==Fe2+ +Cu2+
C.以铜作电极电解硫酸铜溶液:2Cu2+ +2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+
D.AlCl3溶液呈酸性的原因:Al3+ +3H2O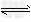 ?Al(OH)3+3H+ ?Al(OH)3+3H+
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列离子方程式书写正确的是( )
A.NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O
B.将氯气通入水中:Cl2+H2O=2H++Cl-+ClO-
C.金属钠与水反应:Na+H2O=Na++OH-+H2↑
D.实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O
参考答案:A.NaHCO3溶液与NaOH溶液反应的离子反应为OH-+H
本题解析:
本题难度:一般
5、选择题 下列离子或化学方程式与所述事实相符且正确的是 [???? ]
A.在氢氧化钡溶液中滴加硫酸氢钾溶液至pH=7:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B.用K37ClO3与浓盐酸反应制氯气:K37ClO3 + 6HCl (浓) K37Cl + 3Cl2↑+ 3H2O K37Cl + 3Cl2↑+ 3H2O
C.向硅酸钠溶液中通入过量的CO2: SiO32- + 2CO2 + 3H2O =H4SiO4↓+ 2HCO3-
D.向AlCl3溶液中滴加过量的氨水:Al3++4OH-=AlO2-+ 2H2O
参考答案:AC
本题解析:
本题难度:一般
|