微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在硫酸的工业制法中,下列对生产操作与生产操作的主要原因的说明都正确的是()
A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能燃烧
B.从沸腾炉出来的炉气需要净化,因为炉气中SO2会与杂质反应
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全
参考答案:D
本题解析:选项A中操作正确,但解释不正确,因为将矿石粉碎的目的是增大矿石与空气的接触面积,使之燃烧充分且完全;B选项的解释不对,因为净化炉气的目的是防止杂质使催化剂中毒和腐蚀管道;C选项的解释不对,因为使用催化剂的目的是加快化学反应的速率,并不能影响化学平衡,也就不能影响转化率。
本题难度:简单
2、选择题
A.二氧化硫
B.氮氧化物
C.二氧化碳
D.悬浮颗粒
参考答案:C
本题解析:城市空气质量日报的内容是二氧化硫、氮氧化物和悬浮颗粒,而二氧化碳不属于此报道内容。
本题难度:简单
3、选择题 向5 mL 18 mol/L的硫酸中加入足量铜片并加热使其充分反应,下列说法正确的是(??)
A.有0.09 mol的硫酸被还原
B.有0.045 mol的硫酸被还原
C.充分反应后体系无硫酸剩余
D.消耗的铜的质量一定小于2.88 g
参考答案:D
本题解析:浓硫酸与铜可发生氧化还原反应,而稀硫酸与铜不反应。浓硫酸与铜反应时,随着反应的进行,浓硫酸的浓度逐渐降低变成稀硫酸,因此实际参加反应的硫酸的量要比理论值小。根据题意可得n(H2SO4)=0.005 L×18 mol・L-1=0.09 mol,参加反应的硫酸n(H2SO4)<0.09 mol,被还原的硫酸小于0.045 mol,参加反应的铜的质量小于2.88 g。
本题难度:一般
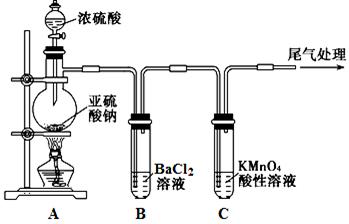
4、实验题 某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
已知:Na2SO3+H2SO4(浓)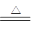 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是??????????????????????。
(2)实验过程中,C中的现象是???????????????????????????????,说明SO2具有??????性。
(3)实验过程中,观察到装置B中出现了明显的白色沉淀。为探究该白色沉淀的成分,该小组同学进行了如下实验:
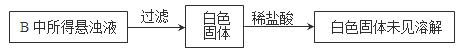
根据实验事实判断该白色沉淀的成分是??????????????(填化学式),产生该白色沉淀的原因可能是????????????(填字母编号)。
a.BaSO3既不溶于水也不溶于酸
b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH
d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3,对此实验是否有影响并明理由???????????????????????????????????????????????????????????????????????????????????。
参考答案:(1)分液漏斗?(2)KMnO4溶液退色?? 还原
(
本题解析:
试题分析:(2)酸性高锰酸钾为强氧化剂,其溶液褪色说明SO2具有还原性;(3)生成的沉淀不溶于盐酸,确定该沉淀为BaSO4,根据题意分析产物只能是SO2的氧化产物,氧化剂只能是空气中的氧气;(4)硝酸具有强氧化性,能把亚硫酸钠氧化为硫酸钠,而得不到SO2气体。
本题难度:一般
5、计算题 硫与热强碱溶液可生成S2-和SO32-;生成物继续与硫作用得S22-和S2O32-。过滤后除去过量硫,向滤液中加入一定量的强碱后,再适入足量的SO2,SO2与S22-也完全转化为S2O32-。问:
 S+SO2+OH-完全转化为S2O32-的离子方程式____________________
S+SO2+OH-完全转化为S2O32-的离子方程式____________________
 amol S最终转化为Na2S2O3,需SO2、NaOH的物质的量分别为________
amol S最终转化为Na2S2O3,需SO2、NaOH的物质的量分别为________
 若amolS最终转化为Na2Sz耗原热碱溶液6molNaOH,则Na2Sx中x值为
若amolS最终转化为Na2Sz耗原热碱溶液6molNaOH,则Na2Sx中x值为
 _________。
_________。
参考答案:
(1) S+SO2+2OH-=S2O32-+H2O?
本题解析:
3S+6OH????△???? 2S2-+SO32-+3H2O?…………①

 ???????? S2-
???????? S2-
本题难度:一般