微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (6分)在某温度下,将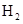 和
和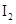 各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定
各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定 的变化,5S时测定
的变化,5S时测定 =0.0080mol/L并保持不变。H2+I2?(g)
=0.0080mol/L并保持不变。H2+I2?(g)  ?2HI(g)
?2HI(g)
(1)反应的平衡常数的表达式是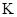 =???????????????????;
=???????????????????;
(2)此温度下,平衡常数值为?????????????????;
(3)若在此温度下,在10L的密闭器充入0.2molHI气体,达到平衡时,HI的转化率为???????。
参考答案:(1) 本题解析:(1)平衡常数是指可逆反应达到化学平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以该反应的平衡常数表达式为
本题解析:(1)平衡常数是指可逆反应达到化学平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以该反应的平衡常数表达式为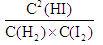 。
。
(2)反应前氢气和碘分子的浓度都是0.01mol/L,5S时测定 =0.0080mol/L,则消耗碘分子的浓度为0.01mol/L-0.008mol/L=0.002mol/L,生成HI是0.004mol/L,所以反应的平衡常数
=0.0080mol/L,则消耗碘分子的浓度为0.01mol/L-0.008mol/L=0.002mol/L,生成HI是0.004mol/L,所以反应的平衡常数
等于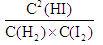 =
=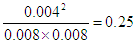
(3)?????????????? 2HI(g)? ??H2???+??? I2?(g)
??H2???+??? I2?(g)
起始量(mol)?????? 0.2??????????? 0???????? 0
转化量(mool)????? 2x???????????? x???????? x
平衡量(mol)???? 0.2-2x????????? x???????? x
逆反应的平衡常数是正反应的倒数
所以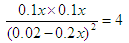
解得x=0.08
所以转化率是2x÷0.2×100%=80%
本题难度:一般
2、填空题 (8分)2A? B + C在某一温度时,达到平衡。
B + C在某一温度时,达到平衡。
(1)?若温度升高,平衡向正反应方向移动,则正反应是___________反应(填放热或吸热);
(2)?若B为固体,降低压强平衡向逆反应方向移动,则A呈___________态;
(3)?若A是气态时,加压时,平衡不移动,则B为_________态,C为__________态;
(4) 若A、B、C均为气体,加入催化剂,平衡___________移动(填正向、逆向、不)
参考答案:(1)?吸热?? (2)气?? (3)?气、气???? (4
本题解析:考查外界条件对平衡的影响。
(1)根据勒夏特列原理可知,?若温度升高,平衡向正反应方向移动,则正反应是吸热反应。
(2)降低压强平衡向逆反应方向移动,则正反应是体积减小的。所以若B为固体,则A一定是气态。
(3)?加压时,平衡不移动,说明反应前后体积不变,所以若A是气态时,B和C一定都是气态。
(4)催化剂只能改变反应速率,但不能改变平衡状态,所以使用催化剂平衡不移动。
本题难度:一般
3、选择题 下列说法不正确的是?
A.在固定体积的密闭容器中发生可逆反应A(s)+B(g) C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
B.对于反应C(s)+CO2(g) 2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
C.向0.1mol・L-1的NH3・H2O中加入氯化铵固体,则溶液中 增大
增大
D.常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液后,溶液中 不变
不变
参考答案:C
本题解析:在反应A(s)+B(g) C(g)+D(g)中, A是固体,反应容器体积固定,故达到平衡前气体的密度随气体质量变化而变化,当气体密度不再改变时,说明已达到化学平衡状态,A正确;△H>0,说明反应C(s)+CO2(g)
C(g)+D(g)中, A是固体,反应容器体积固定,故达到平衡前气体的密度随气体质量变化而变化,当气体密度不再改变时,说明已达到化学平衡状态,A正确;△H>0,说明反应C(s)+CO2(g)  2CO(g)是吸热反应,化学平衡常数增大,说明反应温度升高,因而反应速率也一定增大,B正确;氨水中存在电离平衡:NH3・H2O
2CO(g)是吸热反应,化学平衡常数增大,说明反应温度升高,因而反应速率也一定增大,B正确;氨水中存在电离平衡:NH3・H2O NH4++OH-,加入氯化铵固体后增大了c(NH4+),平衡向左移动,c(OH-)减小而c(NH3・H2O)增大,故
NH4++OH-,加入氯化铵固体后增大了c(NH4+),平衡向左移动,c(OH-)减小而c(NH3・H2O)增大,故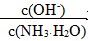
减小,C错误;Mg(OH)2悬浊液中存在着溶解平衡

故
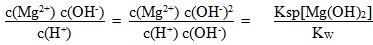 ,
,
而Ksp[Mg(OH)2]与KW均是温度的函数,不随浓度变化而改变,D正确。
本题难度:一般
4、选择题 在一定温度下,在固定容积的密闭容器中,可逆反应H2(g)+ Br2(g)  2HBr(g)达到平衡的标志是
2HBr(g)达到平衡的标志是
A.断裂1 mol H-H键的同时生成2 mol H-Br键
B.单位时间内消耗1 mol H2,同时生成1 mol Br2
C.H2、Br2、HBr的分子数之比为1∶1∶2
D.混合气体的压强不再改变
参考答案:B
本题解析:
试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,据此可以判断。A、根据反应式可知断裂1 mol H-H键的同时一定生成2 mol H-Br键,即二者的反应速率方向一致,因此不能说明反应达到平衡状态,A不正确;B、单位时间内消耗1 mol H2,则必然同时消耗1mol单质溴,由于同时生成1 mol Br2,所以单质溴的正逆反应速率相等,可以说明反应达到平衡状态,B正确;C、平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此H2、Br2、HBr的分子数之比为1∶1∶2不一定是平衡状态,C不正确;D、反应前后体积不变,因此压强始终是不变的,所以压强不变,不能说明反应达到平衡状态,D不正确,答案选B。
本题难度:一般
5、选择题 甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是

A.脱氢反应的△H<0
B.600K时,Y点甲醇的υ(正) <υ(逆)
C.从Y点到Z点可通过增大压强
D.在t?1K时,该反应的平衡常数为8.1mol・L-1
参考答案:BD
本题解析:
试题分析:A中由图像可以看出随着温度升高甲醛平衡转化率升高,说明脱氢反应是吸热反应,故A错误;B中600K时由图像可以看出,Y点所对应的转化率比平衡转化率高,说明此时反应向逆反应方向进行,故甲醇的υ(正) <υ(逆),正确;D中由图像看出转化率为0.9,利用三段法解得:设形如时甲醇的物质的量为1mol,则K=0.9*0.9/0.1=8.1
本题难度:一般